
科目: 来源: 题型:
【题目】《本草图经》中关于绿矾的分解有如下描述:“绿矾形似朴消(Na2SO4·10H2O)而绿色,取此物置于铁板上,聚炭,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金汁者是真也。”对此段话的说明中肯定错误的是
A.绿矾的化学式为FeSO4·7H2O B.绿矾分解过程中没有发生电子的转移
C.“色赤”物质可能是Fe2O3 D.流出的液体中可能含有硫酸
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们认为生活中处处有化学。下列说法正确的是( )
①食盐主要成分为NaCl ②西红柿富含维生素C ③鸡蛋富含蛋白质 ④O2具有可燃性 ⑤肉类富含纤维素
A. ①②④ B. ①③⑤ C. ③④⑤ D. ①②③
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.氯化钠溶液在电流作用下电离成钠离子和氯离子
B.强电解质溶液不一定比弱电解质的导电性强
C.共价键的极性强的化合物一定是强电解质
D.强、弱电解质的导电性只由它们的浓度决定
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米磁性流体材料广泛应用于减震、医疗器械、声音调节等高科技领域。下图是制备纳米Fe3O4磁流体的两种流程:

(1)分析流程图中的两种流程,其中______(填“流程1”、“流程2”)所有反应不涉及氧化还原反应。步骤①反应的离子方程式为____________。
(2)步骤②保持50℃ 的方法是_____________。
(3)步骤③中加入的H2O2电子式是_______,步骤③制备Fe3O4磁流体的化学方程式为_______。
(4)流程2中FeCl3和FeCl2制备Fe3O4磁流体,理论上FeCl3和FeCl2物质的量之比为_____。己知沉淀B为四氧化三铁.步骤⑤中操作a具体的步骤是____________。
(5)利用K2Cr2O7可测定Fe3O4磁流体中的Fe2+含量。若Fe3O4磁流体与K2Cr2O7充分反应消耗了0.01mol·L -1的K2Cr2O7标准溶液100mL,则磁流体中含有Fe2+的物质的量为______mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期生族元素X、Y、Z、W、R原子序数恢次增大.m、p、r是这些元素组成的二元化合物,n、q、s是这些元素组成的三元化合物且属于离子化合物.其中s的水溶液俗称水玻璃。.0. 1mol/Ln溶液的pH为13,m可制作耐火管且属于两性物质。上述物质的转化关系如图所示。下列说法正确的是
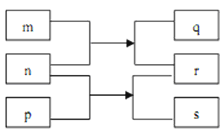
A. 简单气态氢化物的稳定性:R>Y
B. 离子半径大小:Y>Z>W
C. W的最高价氧化物对应的水化物碱性比Z的强
D. 单质的熔点:Z>R>X
查看答案和解析>>
科目: 来源: 题型:
【题目】由单质A与化合物B两种粉末组成的混合物, 在一定条件下可按下图所示发生转化:
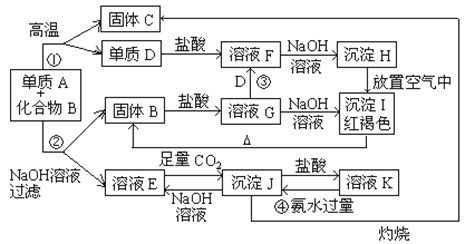
请回答:
(1)A的化学式__________________,B的名称______________________;
(2)反应①的化学方程式________________________________________;
(3)反应②的离子方程式________________________________________;
(4)反应③的离子方程式________________________________________;
(5)反应④的离子方程式________________________________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为0.100mol/LNaOH溶液分别滴定20.00mL0.100mol/L的HA和HB的滴定曲线。下列说法错误的是(己知1g2≈0.3)

A. HB是弱酸,b点时溶液中c(B-)>c(Na+)>c(HB)
B. a、b、c三点水电离出的c(H+): a<b<c
C. 滴定HB时,不宜用甲基橙作指示剂
D. 滴定HA溶液时,当V(NaOH)=19.98mL时溶液pH约为3.7
查看答案和解析>>
科目: 来源: 题型:
【题目】下列应用不涉及氧化还原反应的是
A.Na2O2用作呼吸面具的供氧剂 B.工业上电解熔融状态Al2O3制备Al
C.工业上利用合成氨实现人工固氮 D.实验室用NH4Cl和Ca(OH)2制备NH3
查看答案和解析>>
科目: 来源: 题型:
【题目】锂离子电池在各种电子产品中广泛使用,某种可充电的锂离子电池的装置如图所示(a极材料为金属锂镶嵌在石墨中的复合材料),总反应方程式是FePO4(s)+Li(s)![]() LiFePO4(s)。下列说法正确的是
LiFePO4(s)。下列说法正确的是
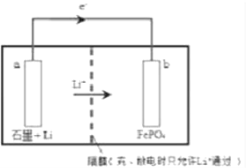
A. 根据图示可以判断该电池处于充电状态
B. 在放电状态时,a是正极,充电时a是阳极
C. 该电池中a、b极都可以接触水溶液
D. 充电时,b极的电极反应式是LiFePO4-e-=Li++FePO4
查看答案和解析>>
科目: 来源: 题型:
【题目】现有周期表中前四周期的五种元素A、B、C、D、E,其中A、B、C为金属且位于同一周期,原子序数C>B>A;A、C核外均没有未成对电子;B被誉为“21世纪的金属”,B原子核外有二个未成对电子和三个空轨道;D原子最外层电子数是其周期序数的三倍;E能与D形成化合物ED2,可用于自来水的消毒。
(1)B元素基态原子的电子排布式为_______,E元素在周期表中的位置为_______。
(2)化合物E2D分子的立体构型为________,中心原子采用_______杂化。
(3)B与E能形成一种化合物BE4,其熔点:-25℃,沸点:136.4℃。则该化合物属于____晶体,晶体内含有的作用力类型有_______。
(4)A、B、D三种元素形成的某晶体的晶胞结构如图,则晶体的化学式为______。若最近的B 与D的原子距离为acm,该物质的摩尔质量为Mg/mol,阿伏加德罗常数的数值为NA,则该晶体的密度为_______g/cm3。
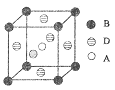
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com