
科目: 来源: 题型:
【题目】下面是几种常见的化学电源示意图,有关说法不正确的是( )
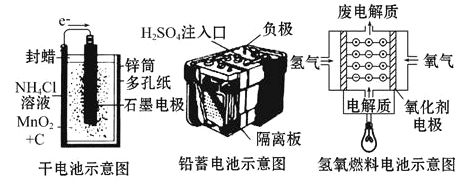
A. 上述电池分别属于一次电池、二次电池和燃料电池
B. 干电池在长时间使用后,锌筒被破坏
C. 氢氧燃料电池是一种具有应用前景的绿色电源
D. 铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
查看答案和解析>>
科目: 来源: 题型:
【题目】[选修5:有机化学基础](20分)
Ⅰ(6分)
香茅醛(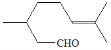 )可作为合成青蒿素的中间体,关于香茅醛的叙述正确的有
)可作为合成青蒿素的中间体,关于香茅醛的叙述正确的有
A.分子式为C10H18O B.不能发生银镜反应
C.可使酸性KMnO4溶液褪色 D.分子中有7种不同化学环境的氢
Ⅱ(14分)
当醚键两端的烷基不相同时(R1-O-R2,R1≠R2),通常称其为“混醚”。若用醇脱水的常规方法制备混醚,会生成许多副产物:
R1—OH+ R2—OH ![]() R1—O—R2+ R1—O—R1+ R2—O—R2+H2O
R1—O—R2+ R1—O—R1+ R2—O—R2+H2O
一般用Williamson反应制备混醚:R1—X+ R2—ONa→R1—O—R2+NaX,某课外研究小组拟合成![]() (乙基苄基醚),采用如下两条路线进行对比:
(乙基苄基醚),采用如下两条路线进行对比:
Ⅰ:![]()
Ⅱ:①![]()
②![]()
③![]()
回答下列问题:
(1)路线Ⅰ的主要副产物有______________、______________。
(2)A的结构简式为______________。
(3)B的制备过程中应注意的安全事项是______________。
(4)由A和B生成乙基苄基醚的反应类型为______________。
(5)比较两条合成路线的优缺点:______________。
(6)苯甲醇的同分异构体中含有苯环的还有________种。
(7)某同学用更为廉价易得的甲苯替代苯甲醇合成乙基苄基醚,请参照路线Ⅱ,写出合成路线______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】[选修3:物质结构与性质](20分)
Ⅰ(6分)下列叙述正确的有
A.某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7
B.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能
C.高氯酸的酸性与氧化性均大于次氯酸的酸性和氧化性
D.邻羟基苯甲醛的熔点低于对羟基苯甲醛的熔点
Ⅱ(14分)ⅣA族元素及其化合物在材料等方面有重要用途。回答下列问题:
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为___________,原子间存在的共价键类型有________,碳原子的杂化轨道类型为__________________。

(2)SiCl4分子的中心原子的价层电子对数为__________,分子的立体构型为________,属于________分子(填“极性”或“非极性”)。
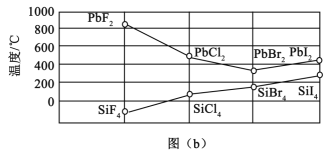
(3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。
①SiX4的沸点依F、Cl、Br、I次序升高的原因是_________________。
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性_______、共价性_________。(填“增强”“不变”或“减弱”)
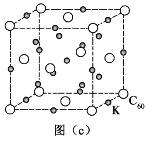
(4)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为_______________;其晶胞参数为1.4 nm,晶体密度为_______g·cm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】能正确表达下列反应的离子方程式为
A.用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
B.硫化亚铁与浓硫酸混合加热:2H++FeS=H2S↑+ Fe2+
C.向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3![]() =Al2(CO3)3↓
=Al2(CO3)3↓
D.用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH-=![]() +
+![]() + H2O
+ H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 由NaH2PO2是正盐可推知H3PO2是一元酸
B. 由同种元素组成的物质一定是纯净物
C. 直径介于1~100nm之间的微粒称为胶体
D. 不能与酸反应生成盐和水的氧化物,能够与碱反应生成盐和水
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:

①上述分类中,分成A、B两组的依据是___________________________;
②C组物质与水反应的离子方程式为________________________________;
③D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有__________(填化学式)。
(2)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:
A.Na2O2+2HCl===2NaCl+H2O2
B.Ag2O+H2O2===2Ag+O2↑+H2O
C.2H2O2===2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O
①上述反应中,H2O2既体现氧化性又体现还原性的反应是____________;
②保存过氧化氢的试剂瓶上最适合贴上的一个标签是________(填序号);

③H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN)。H2O2被称为绿色氧化剂的理由是___________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
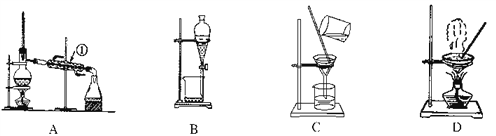
(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________。
(2)从油水混合物中分离出植物油,选择装置________,该分离方法的名称为________。
(3)装置A中①的名称是________,进水的方向是从________口进水。装置B在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是______________________。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
粗盐中含Ca2+、Mg2+、Fe3+、SO![]() 等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是________(填选项字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A. BaSO4溶于水的部分能够电离,所以BaSO4是电解质
B. SO2的水溶液能够导电,所以SO2是电解质
C. 液态Cl2不导电,所以Cl2是非电解质
D. 液态HCl不导电,所以HCl是非电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com