
科目: 来源: 题型:
【题目】臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g) ![]() N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A | B | C | D |
|
|
|
|
升高温度,平衡常数减小 | 0~3 s内,反应速率为v(NO2)= 0.2 mol·L-1 | t1时仅加入催化剂,平衡正向移动 | 达到平衡时,仅改变x,则x为c(O2) |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】向甲、乙两个容积均为1 L的恒容容器中,分别充入2 mol A、2 mol B和1 mol A、1 mol B。相同温度下发生反应:A(g)+B(g) ![]() xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示。下列说法正确的是( )
xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示。下列说法正确的是( )


A. x可能等于1
B. 甲、乙两容器中反应达平衡时,平衡常数K甲<K乙
C. 将乙容器升温可使甲、乙容器内各物质的体积分数相同
D. 若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 mol·L-1<c(A)<1.56 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积为2 L的3个密闭容器中发生反应3A(g)+B(g)![]() xC(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
xC(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 3 mol A、2 mol B | 6 mol A、4 mol B | 2 mol C |
到达平衡的时间/min | 5 | 8 | |
A的浓度/(mol·L-1) | c1 | c2 | |
C的体积分数 | w1 | w3 | |
混合气体密度/(g·L-1) | ρ1 | ρ2 |
下列说法正确的是 ( )
A. 若x<4,则2c1<c2 B. 若w3=w1,可断定x=4
C. 无论x的值是多少,均有2ρ1=ρ2 D. 容器甲中反应从开始到达平衡平均速率为v(A)=0.3 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】有X、Y两种原子,X原子的M电子层比Y原子的M电子层少3个电子,Y原子的L电子层的电子数恰好为X原子L电子层电子数的2倍,X和Y分别是
A.碳和铝B.硅和钠C.硼和氮D.氯和碳
查看答案和解析>>
科目: 来源: 题型:
【题目】做化学实验必须注意实验安全。下列做法正确的是
A. 金属钠保存在四氯化碳中 B. 制氯气在通风橱中进行
C. 金属钠着火用小苏打干粉灭火 D. 发生火灾拨打110报警电话
查看答案和解析>>
科目: 来源: 题型:
【题目】氯气是一种化学性质活泼的气体。(1)新制备的氯水呈浅黄绿色,说明氯水中有 分子存在(写化学式)。向氯水中滴入几滴AgNO3溶液,现象是 。
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察的现象是 。
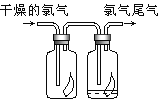
(3)为防止氯气污染空气,可用 溶液吸收多余的氯气,该反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成SO3
C. 加入催化剂有利于氨的合成
D. 工业制取金属钾Na(l)+KCl(l)![]() NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
查看答案和解析>>
科目: 来源: 题型:
【题目】在2 L密闭容器中通入a mol X气体并发生反应:2X(g) ![]() Y(g),在T1、T2温度下,X的物质的量n(X)随时间t变化的曲线如图所示。下列叙述不正确的是( )
Y(g),在T1、T2温度下,X的物质的量n(X)随时间t变化的曲线如图所示。下列叙述不正确的是( )
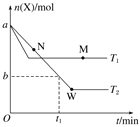
A. 正反应方向为放热反应
B. 在T2温度下,在0~t1时间内,v(Y)=![]() mol·L-1·min-1
mol·L-1·min-1
C. M点的正反应速率v正大于N点的逆反应速率v逆
D. W点时再加入一定量X,平衡后X的转化率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】高锰酸钾是一种典型的强氧化剂。
完成下列填空:
Ⅰ.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO4-+ Cu2S + H+→ Cu2+ + SO2↑ + Mn2++ H2O(未配平)
② MnO4-+ CuS + H+ → Cu2+ + SO2↑ + Mn2++ H2O(未配平)
(1)下列关于反应①的说法中错误的是 (选填编号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24 L(标况下) SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是: Mn2+> Cu2S
(2)标出反应②中电子转移的方向和数目: MnO4-+ CuS
Ⅱ.在稀硫酸中,MnO4-和H2O2也能发生氧化还原反应
氧化反应:H2O2-2e → 2H++ O2↑
还原反应:MnO4- + 5e + 8H+→ Mn2++ 4H2O
(3)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为 。由上述反应得出的物质氧化性强弱的结论是 >___________(填写化学式)。
(4)已知:2KMnO4+ 7H2O2+3H2SO4→ K2SO4+2MnSO4+6O2↑+10H2O,则被1mol KMnO4氧化的H2O2是
mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com