
科目: 来源: 题型:
【题目】下列说法正确的是
A. 离子键就是使阴、阳离子结合成化合物的静电引力
B. 所有金属与所有非金属之间都能形成离子键
C. 含有共价键的化合物一定是共价化合物
D. 含有离子键的化合物一定是离子化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,可逆反应 A(g)+ 3B(g)2C(g)达到平衡的标志是
A.C 的生成速率与 B 的生成速率相等
B.单位时间生成 nmolA,同时生成 3nmolB
C.A、B、C 的浓度不再变化
D.A、B、C 的分子数比为 1:3:2
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种。若将甲溶液滴入乙溶液中,无明显现象发生,甲溶液滴入丙溶液时,发现有白色沉淀生成,继续滴加则沉淀消失。据此可推断丁物质是
A. Al2(SO4)3 B. FeSO4
C. NaOH D. BaCl2
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上真空炼铷的原理为2RbCl+Mg ![]() MgCl2+2Rb(g),下列说法正确的是
MgCl2+2Rb(g),下列说法正确的是
A. 镁的金属活动性比铷强,故镁可置换铷
B. 铷的沸点比镁低,把铷蒸气抽出时,平衡右移
C. MgCl2的热稳定性比RbCl弱
D. Rb单质比RbCl更稳定
查看答案和解析>>
科目: 来源: 题型:
【题目】现有三种可溶性物质A、B、C,其中A、B是盐,C是碱,它们溶于水后电离产生的所有离子如下表所示:
阳离子 | Na+ H+ Ba2+ |
阴离子 | OH- CO32- SO42- |
请根据下列叙述回答问题:
(1)C的化学式为_____________。
(2)A溶液与B溶液反应可生成气体X,则X的化学式为_______,该反应的离子方程式为____________________________________。
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸。
①B的化学式为____________,如何鉴别B中的阴离子________________________。
②D溶于稀硝酸的离子方程式为____________________________________________。
③D与E的混合物a克,加入足量盐酸,完全反应生成的气体在标准状况下体积为b升,求E在混合物中的质量分数 _____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】香兰素是重要的香料之一,它可由丁香酚经多步反应合成。
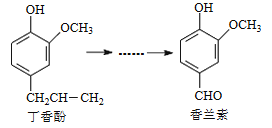
有关上述两种化合物的说法错误的是
A. 丁香酚与香兰素都能与H2发生加成反应
B. 常温下,1 mol丁香酚最多消耗1 mol Br2
C. 丁香酚和香兰素遇FeCl3溶液都能发生显色反应
D. 常温下,丁香酚与香兰素都能与浓溴水发生反应
查看答案和解析>>
科目: 来源: 题型:
【题目】X元素原子的L层比Y元素原子的L层少3个电子,X元素原子的核外电子总数比Y原子核外电子总数少5个,则X、Y可形成的化合物是
A. 离子化合物Y(XO4)2 B. 离子化合物Y2X3
C. 共价化合物XY2 D. 离子化合物Y3X2
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸工业是我国化工生产支柱产业。主要生产工艺流程如下:

接触室中的反应为2SO2(g)+O2(g)![]() 2SO3(g) H=197 kJ·mol1。
2SO3(g) H=197 kJ·mol1。
请回答以下几个问题:
(1)图中炉气要净化的原因是_____________________________________。
(2)吸收塔排出的尾气先用足量的氨水吸收,反应的离子方程式为_______________,再用浓硫酸处理,得到较高浓度的SO2和铵盐。所得的SO2可用于工业制溴过程中吸收潮湿空气中的Br2,吸收Br2的过程中主要反应的化学方程式是____________________________________。所得铵盐溶液中各离子物质的量浓度由大到小的顺序为________________________。
(3)为什么从接触室出来的SO3气体不用水直接吸收,而是用98.3%的浓硫酸吸收:____________________。
![]() (4)燃烧1 t含二硫化亚铁90%的黄铁矿,在理论上能生产________t 98%的硫酸(设有1.5%的硫留在炉渣里,精确至0.01),从提高SO3的产率同时适当降低生产成本的角度出发,以下措施可取的是___________(填字母)。
(4)燃烧1 t含二硫化亚铁90%的黄铁矿,在理论上能生产________t 98%的硫酸(设有1.5%的硫留在炉渣里,精确至0.01),从提高SO3的产率同时适当降低生产成本的角度出发,以下措施可取的是___________(填字母)。
A.通入过量的空气 B.使用优质催化剂
C.调整适宜的温度 D.采用高压
(5)科研工作者开发了制备SO2,再用电化学原理生产硫酸的方法,装置如图。为了稳定技术生产,硫酸的浓度应维持不变,则通入的SO2和水的质量比为__________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com