
科目: 来源: 题型:
【题目】实验室里利用以下反应制取少量氮气:NaNO2+NH4Cl===NaCl+N2↑+2H2O。关于该反应的下列说法正确的是( )
A. 每生成1 mol N2转移的电子的物质的量为6 mol
B. N2既是氧化剂,又是还原剂
C. NH4Cl中的氮元素被还原
D. NaNO2是氧化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示。A为含硫氮正盐其中硫元素化合价为+4,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝。试回答下列问题:

(1)写出下列物质化学式:D:__________;F:__________。
(2)写出下列反应的离子方程式:
①A和酸性KMnO4溶液反应__________;
②D和新制氯水:__________。
(3)通过本题的解答,在检验SO42-时,应使用__________。
A.盐酸酸化的BaCl2溶液 B.硝酸酸化的Ba(NO3)2溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某酸性溶液中存在较多的Cu2+、NO3-,则该溶液中还可能大量存在的离子组是( )
A. OH-、CO32-、Na+ B. ClO-、HCO3-、K+
C. SO42-、Cl-、NH4+ D. Br-、Fe2+、Ba2+
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上真空炼铷的原理为2RbCl+Mg ![]() MgCl2+2Rb(g),下列说法正确的是
MgCl2+2Rb(g),下列说法正确的是
A. 镁的金属活动性比铷强,故镁可置换铷
B. 铷的沸点比镁低,把铷蒸气抽出时,平衡右移
C. MgCl2的热稳定性比RbCl弱
D. Rb单质比RbCl更稳定
查看答案和解析>>
科目: 来源: 题型:
【题目】核电荷数由小到大顺序排列的五种短周期元素X、Y、Z、W、Q,其中在同周期中,Z的金属性最强,Q的非金属性最强;W的单质是淡黄色固体;X、Y、W在周期表中的相对位置关系如图所示
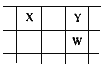
(1)五种元素形成的单质,其中固态时属于原子晶体的是________(填化学式);常用作强氧化剂的是________、________(填化学式)。
(2)这五种元素中,原子半径最大的是________(填化学式);由Z、W、Q形成的简单离子半径由大到小的顺序是________(用化学式表示);X、W、Q的最高价氧化物的水化物酸性从强到弱的顺序是________(用化学式表示)。
(3)Y和Z形成的一种化合物中含有离子键和共价键,请用电子书表示该化合物中化学键的形成过程___________________________________。
(4)Z与Q反应生成的化合物属于________化合物;电解该化合物的饱和溶液,阳极的电极反应式为________;电解一段时间后,将阳极产物和阴极溶液混合,反应的化学方程式是______________。
(5)由X、Y和氢三种元素组成的化合物X6H12Y6,已知:9 g该化合物燃烧放出140 kJ的热,写出该化合物燃烧热的热化学方程式:_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)19.2g SO2在标准状况下的体积为______,其中含氧原子的物质的量为______,该气体在标准状况下的密度是______(若不能整除,保留两位小数)。
(2)0.5mol H3PO4质量是_______,含______个H3PO4分子,含______mol氧原子。
(3)在标准状况下,将体积为______ NH3溶于水得到0.5 mol·L-1的氨水500 mL;配制100 mL 0.1 mol·L-1CuSO4溶液,需要CuSO4·5H2O质量为________。
(4)现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
①同温同压下,M、N气体的密度之比为____________;
②相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】图为实验室某盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为______mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______;
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为 0.400mol·L-1的稀盐酸。
①容量瓶上需标有以下五项中的________。
A.温度 B.浓度 C.容量 D.压强 E.刻度线
②将下列操作填写完整,并排列其正确的操作顺序________(用字母表示,每个字母只能用一次);
A.用少量蒸馏水洗涤________2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。
B.用量筒准确量取浓盐酸 ________mL,注入烧杯中,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其混合均匀。
C.将已冷却的盐酸沿玻璃杯注入________中。
D.盖好瓶塞,颠倒摇匀,装瓶,贴签。
E.改用__________加水,至_____________________________。
F.继续往容量瓶内小心加水,直到液面接近刻度________处。
③在配制过程中,下列实验操作对所配制的稀盐酸物质的量浓度有何影响? (在横线上天“偏大”、“偏小”、“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面__________;
b.洗涤量取浓盐酸后的量筒,并将洗涤液转移到容量瓶中__________;
c.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水___________;
d.定容时仰视刻度线__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】装置(Ⅱ)的主要缺点是___________________________________,如果选用此装置来完成实验,则必须采取的改进措施是:______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com