
科目: 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以I—的形式存在。实验室里从海带中提取碘的流程如下:(已知C12+2KI=2KCl+I2)
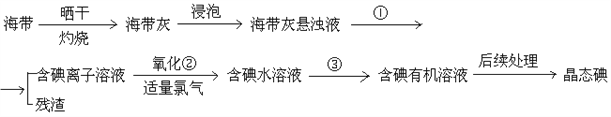
(1)步骤①的操作方法是________;除漏斗、烧杯外,还需要使用的玻璃仪器是__________。
(2)提取碘的过程中,可供选择的萃取剂是(______)
A、苯、酒精 B、CCl4、苯 C、汽油、醋酸
(3)步骤③的操作中,所用的主要玻璃仪器是_________________。当将含碘有机溶液静置分层后,若要取出下层液体的接下来的操作是:________________________________________
(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏过程,蒸馏实验中用到的主要玻璃仪器有:温度计、牛角管、酒精灯、____________、__________、锥形瓶。
查看答案和解析>>
科目: 来源: 题型:
【题目】用98%的浓硫酸(其密度为1.84 g/cm3)配制100 mL 1.0 mol·L-1稀硫酸,
实验步骤如下:① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解 ④检漏、 转移、洗涤 ⑤ 定容、摇匀
若实验仪器有:A.100 mL量筒 B.托盘天平 C.玻璃棒 D.50 mL容量瓶 E.10 mL量筒 F.胶头滴管 G.50 mL烧杯 H.100 mL容量瓶
回答下列问题:
(1)需量取浓硫酸的体积为__________mL。
(2)实验时选用的仪器有(填序号) _______________,
(3)配制过程中,下列情况会使配制结果偏高的是(填序号) _______________
①定容时仰视刻度线观察液面 ②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,未再加蒸馏水补至刻度线
④.所用的浓硫酸长时间放置在密封不好的容器中⑤用量筒量取浓硫酸时仰视读数
(4)检验试剂瓶中的溶液含有SO42- 的操作是____________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质混合后,没有明显现象的是( )
①H2S和SO2 ②SO2和SO3
③SO2和氯水 ④SO3(气)和Cl2
⑤H2S和SO3(气) ⑥H2S和Cl2
A. ①③⑥ B. ②④
C. ②⑤⑥ D. ③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如右图所示。利用标签所提供的信息,回答下列问题:

(1)该注射液中葡萄糖的质量分数为___________
(2)葡萄糖分子的摩尔质量________________
(3)该注射液中溶质与溶剂的分子个数比为_______
(4)该注射液中溶质的物质的量浓度为________(小数点后保留2位)
(5)已知室温下,饱和葡萄糖水溶液中溶质的质量分数为51.3%, 请计算室温下葡萄糖的溶解度____________ (保留小数点后1位)。
(6)若在实验室利用葡萄糖固体配制该注射液( 500mL5%葡萄糖)在没有容量瓶的情况下,能否配制上述溶液?______,若不能说明理由,若能说明配制步骤__________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】安全重于泰山,在实验室点燃可燃物更要注意安全。如图是某同学设计的一个可燃性气体安全点燃装置(夹持装置已略去),对此装置的评价和使用错误的是( )

A. 用此装置点燃可燃性气体可防止爆炸的发生
B. 此装置适用于难溶于水的可燃性气体的点燃
C. 此装置防止气体爆炸的原理是使导管内的气体与燃着的气体不直接接触
D. 实验时水槽中水量的多少不会影响实验效果
查看答案和解析>>
科目: 来源: 题型:
【题目】用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1)应称取Na2CO3·10H2O晶体的质量________。
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列问题:(用“偏大”“偏小”或“无影响”填空)
A. Na2CO3·10H2O晶体失去了部分结晶水 ________。
B. 称量碳酸钠晶体时所用砝码生锈 ________
C. 容量瓶未经干燥使用 ________
D. 转移到容量瓶的过程中,有少量的溶液溅出________。
E.定容时,加水超过刻度线,用胶头滴管吸取多余的液体至刻度线________。
(3)下列操作中,容量瓶所不具备的功能有________(填选项字母)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(4)某同学改用固体Na2CO3配制上述Na2CO3溶液的过程如图所示:
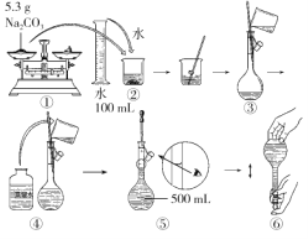
你认为该同学的错误步骤有________(填序号)。
A.1处 B.2处
C.3处 D.4处
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. IA族元素的金属性比IIA族元素的金属性强
B. 第三周期元素的离子半径从左到右逐渐减小
C. 同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D. ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10﹣2,K2=5.4×10﹣5.草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水.草酸晶体(H2C2O42H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解.回答下列问题:
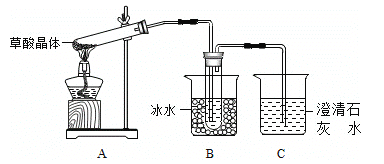
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是 ,由此可知草酸晶体分解的产物中有 .装置B的主要作用是 。
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和如图所示的部分装置(可以重复选用)进行实验.
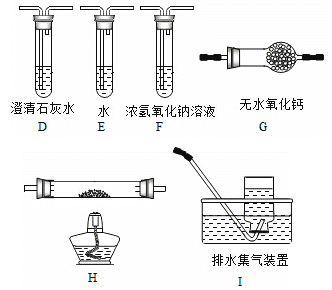
①乙组同学的实验装置中,依次连接的合理顺序为A、B、 装置H反应管中盛有的物质是 。
②能证明草酸晶体分解产物中有CO的现象是
(3)①设计实验证明:
①草酸的酸性比碳酸的强
②草酸为二元酸
查看答案和解析>>
科目: 来源: 题型:
【题目】铁及其化合物在日常生产生活中用途广泛。利用FeSO4制备还原铁粉的工业流程如下:

实验室中可用FeSO4(用铁粉和稀硫酸反应制得)和NH4HCO3在如下装置模拟上述流程中的“转化”环节。

(1)装置A的名称是________,装置B中盛放的试剂是________,NH4HCO3盛放在装置________中。
(2)实验过程中,欲将生成的FeSO4溶液和NH4HCO3溶液混合制FeCO3沉淀,操作方法是________________,发生主要反应的离子方程式为_____________________。FeSO4溶液要现用现配制的原因是____________,检验久置的FeSO4是否变质的方法是______________。
(3)干燥过程主要目的是脱去游离水,过程中会有少量FeCO3在空气中被氧化为FeOOH,该反应的化学方程式为____________________________,取干燥后的FeCO3样品12.49 g,与碳混合后焙烧,最终得到还原铁粉6.16 g,计算样品中杂质FeOOH的质量:________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com