
科目: 来源: 题型:
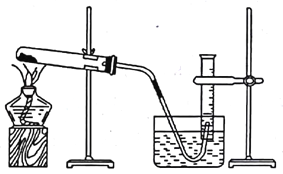
【题目】某同学利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量。实验步骤如下:
①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为ag。
②装好实验装置。
③检查装置气密性。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热(如图所示,导管出口高于液面)。
⑥测量收集到的气体的体积。
⑦准确称量试管和残留物的质量为bg。
⑧测量实验室的温度。
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。
⑩处理实验数据,求出氧气的摩尔质量。
回答下列问题:
(1)如何检查装置的气密性? ____________________
(2)以下是测量收集到的气体体积必须包括的几个步骤:
①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是(请填写步骤代号)_________
(3)如果实验中得到的氧气体积是cL(已换算为标准状况),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含a、b、c,不必化简)M(O2)=__________
查看答案和解析>>
科目: 来源: 题型:
【题目】己知:①CO的结构式为C![]() O;②298K时相关化学键的键能数据如下表:
O;②298K时相关化学键的键能数据如下表:
化学键 | H—H | O—H | C—H | C |
E/(KJ·mol-1) | 436 | 465 | 413 | 1076 |
则反应 CO(g)+3H2(g)![]() CH4(g)+H2O(g)的△H的值为
CH4(g)+H2O(g)的△H的值为
A. -198kJ·mol-1 B. +267 kJ·mol-1 C. -298 kJ·mol-1 D. +634 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】生物学家借助新的显微技术,成功观察到小于200纳米的粒子。下列分散系中,分散质粒子半径最小的是( )
A. 雾 B. 蛋白质溶液 C. 石灰乳 D. KNO3溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 方程式2C+SiO2 ![]() 2CO+Si表明非金属性:碳>硅
2CO+Si表明非金属性:碳>硅
B. 一定量的氯气与过量的铁粉在密闭容器中充分反应,有FeCl2生成
C. 将少量的浓硝酸滴入盛有过量的铜粉的试管中,气体产物只有NO2
D. 向新制备的饱和氯水中加入碳酸钙粉末可以增强氯水的漂白性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 某物质的溶解性为难溶,则该物质不溶于水
B. H2S为二元弱酸,其电离方程式为:H2S![]() 2H++S2-
2H++S2-
C. 已知:常温下,AgCl的Ksp=1.8×10-10。向99mL 0.01 mol/L KCl溶液中,加入lmL 0.01mol/LAgNO3溶液(忽略混合时溶液体积的变化),立即产生白色沉淀
D. NaHCO3溶于水会水解,该水解反应可表示为:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】关于氢键,下列说法正确的是( )
A.每一个水分子内都含有两个氢键
B.H2O分子之所以非常稳定,就是由于氢键所致
C.氢键只能存在于同种物质分子之间(如:HF、H2O、NH3等各自分子之间)
D.冰和水中都有氢键
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关工业生产的叙述正确的是
A. 反应2SO2+O2![]() 2SO3使用催化剂可以提高SO2的转化率
2SO3使用催化剂可以提高SO2的转化率
B. 电解法精炼铜时,同一时间内阳极溶解的铜的质量比阴极析出的铜的质量小
C. 合成氨工业中,通常将液态氨及时分离出去以加快化学反应速率
D. 工业上通常采用电解饱和食盐水的方法制备金属钠
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上在高温高压催化剂条件下合成氨,其反应为
N2(g)+3H2(g)![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
(1)原料气之一的N2不能用空气代替,而必须用纯N2,其原因除了为加快反应速率外还有:
①_____________;
②_____________;
另一原料气H2往往来源于水和焦炭,写出相关的化学方程式_________________。
(2)将N2和H2按1:3体积比(同温同压下)充入合成塔,一段时间后,合成塔内压强变为起始时压强的80%,则此反应过程中N2的转化率为_________(用百分数表示),如其它条件不变,将两气体的体积比调整为1:4,该反应的平衡常数_______(填“不变、变大、变小”)。
(3)合成的氨气可用于合成硝酸进而生产常用化肥NH4NO3,请写出NH4NO3水溶液中各离子浓度由大到小的顺序___________。
(4)将过量氨水滴入CuSO4溶液中先后出现生成沉淀、沉淀溶解的现象。请写出沉淀溶解的离子方程式____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.某一在水溶液中进行的反应体系中,有反应物和生成物共六种物质,这六种物质是: HCl(浓)、KMnO4、MnCl2、H2O、Cl2、 KCl,已知Cl2、KCl 为生成物。
(1)该反应中的氧化剂是_______(写化学式),氧化产物为____ (写化学式),该反应中,氧化产物与还原产物的物质的量之比为__________
(2) 写出该反应的离子方程式:________________
(3) 用单线桥表示该反应电子转移的方向和数目。______________
(4)HCl 在上述反应中体现出米的性质是___________
(5)用该反应制得了标况下560mLCl2,则被氧化的物质为_____mol,转移电子数为______NA(NA表示阿伏伽德罗常数的值)。
Ⅱ.高锰酸钾标准溶液经常用来滴定测量物质的含量。用高锰酸钾法闻接测定石灰石中CaCO3的含量的方法为: 称取试样0.1250g,用稀盐酸溶解后加入(NH4)2C2O4得CaC2O4沉淀。沉淀经过滤洗涤后溶于稀硫酸中。滴定生成的H2C2O4 用去浓度为0.0 16mo/LKMnO4 溶液25.00mL。
(1)写出CaC2O4沉淀溶解的离子方程式:___________________
(2)配平并完成下列高锰酸钾滴定草酸反应的离子方程式:_____________
口MnO4-+ 口H2C2O4+H+=口Mn2++口CO2↑+口
(3)①石灰石中CaCO3的百分含量:_______
②滴定反应中产生的标准状况下的CO2气体为_____mL (保留两位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com