
科目: 来源: 题型:
【题目】在常温下,用0.1000 mol/L的盐酸滴定25 mL 0.1000 mol/L Na2CO3溶液,所得滴定曲线如下图所示。下列有关滴定过程中溶液相关微粒浓度间的关系不正确的是
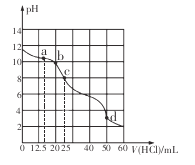
A. a点:c( HCO3-)>c(Cl-)>c(C032-)
B. b点:c(Na+)+c(H+)=c(Cl一)+c(HCO3-)+c(CO32-)+c(OH-)
C. c点:c(OH-)+c(CO32-)=c(H+)+c(H2CO3)
D. d点:c(Cl-)=c(Na+)
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:

已知:①A核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1 mol D可与1 mol NaOH或2 mol Na反应。
回答下列问题:
(1)A生成C的化学方程式为____________________________。
(2)C的官能团名称为____________。
(3)D的结构简式为_________________。
(4)由E生成F的反应类型为____________。
(5)L是D的同分异构体,可与FeCl3溶液发生显色反应,1 mol的L可与1 mol的Na2CO3反应,L核磁共振氢谱为四组峰,峰面积比为3∶2∶2∶1,L的结构简式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下0.1molL-1的二元酸H2A溶液中,溶液中可能存在的含A料子(H2A、HA-、A2-)的物质的量分数(δ)随pH变化的关系如图所示,下列说法正确的是( )
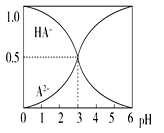
A. H2A的电离方程式为:H2AH++HA-
B. pH=5时,在NaHA和Na2A的混合溶液中:c(HA-):c(A2-)=1:100
C. 等物质的量浓度的NaHA和Na2A溶液等体积混合,离子浓度大小关系为c(Na+)>c(HA-)>c(A2-)
D. Na2A溶液必存在c(OH-)=c(H+)+c(HA-)+2c(H2A),各粒子浓度均大于0
查看答案和解析>>
科目: 来源: 题型:
【题目】空气质量的好坏与空气中氮、硫氧化物的含量有着重要的关联,控制氮、硫氧化物的排放有利于改善空气质量。
(1)目前我国已对许多大型燃煤发电厂进行“脱硝(使NOx转化为N2)”工艺改造,这有利于氮元素在自然界中实现良性循环,“脱硝”涉及到的部分反应如下:
①4NH3(g)+6NO(g) ![]() 5N2(g)+6H2O(g) △H1=-1776kJ·mol-1;
5N2(g)+6H2O(g) △H1=-1776kJ·mol-1;
②8NH3(g)+6NO2(g) ![]() 7N2(g)+12H2O(g) △H2;
7N2(g)+12H2O(g) △H2;
又知:③N2(g)+O2(g) ![]() 2NO(g) △H3=+180kJ·mol-1;
2NO(g) △H3=+180kJ·mol-1;
④2NO(g)+O2(g) ![]() 2NO2(g) △H4=-114kJ·mol-1
2NO2(g) △H4=-114kJ·mol-1
则△H2=__________。
(2)氨的催化氧化是硝酸工业中最重要的一个反应:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) △H=-905kJ·mol-1;一定温度下,向2L某恒容密闭容器充入一定量的NH3、O2,测得NO与某种物质a的浓度与时间的关系如图1所示。
4NO(g)+6H2O(g) △H=-905kJ·mol-1;一定温度下,向2L某恒容密闭容器充入一定量的NH3、O2,测得NO与某种物质a的浓度与时间的关系如图1所示。
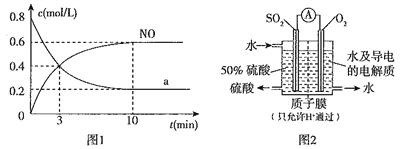
①物质a是___________,前3 min内用H2O表示的平均反应速率v(H2O)=____________。
②若最初通入的O2物质的量为3.3mol,则该温度下反应的平衡常数的值为________。
③下列各项数据中能表明该反应已达到化学平衡状态的是_________(填选项字母)。
a. NH3与NO的生成速率相等 b.混合气体的密度保持不变
c. △H 保持不变 d.容器的总压强保持不变
(3)将NO2、NO混合气体用碱吸收可得到重要的化工产品NaNO2,已知常温下K(HNO2)=5×10-4,则5mol/L的NaNO2溶液的pH=________。
(4)消除SO2污染的方法之一是利用电化学法可直接将其转化为硫酸,转化原理如图2所示,则负极上的电极反应式为____________________________,质子的移动方向为____________________(填“自左向右”或“自右向左”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】观察下列实验装置图,按要求作答:
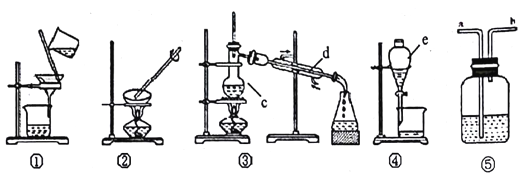
(1)装置中c、d、e的名称分别为_________
(2)分离下列物质,需要在哪套装置中进行?
I.干燥H2,可采用______(填装置序号)装置
II.除去食盐溶液中的水,可采用_____(填装置序号)装置
III. 淡化食盐水,可采用___(填装貿序号)装置
IV.实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可采用____(填装置序号)装置除去Ca(OH)2溶液中悬浮的CaCO3微粒
V.分离碘水中的碘应先选择装置_____(填装置序号),进行______和____操作,再用装置____(填装置序号)进行______操作。
查看答案和解析>>
科目: 来源: 题型:
【题目】用生石灰(CaO)、纯碱(Na2CO3)和食盐(NaCl)按一定比例混合可制得一种腌制原料,某同学为了探究该原料成份做了以下实验:
该同学取一定量的样品溶于水,主要发生的化学方程式有:____________________________, _____________________________________。
(2)该同学认为(1)过滤后所得的滤液中肯定含有大量的NaOH、NaCl溶质,还可能含有Ca(OH)2或Na2CO3 ,为了探究所得滤液中可能含有的物质是否存在,请你帮他完善实验方案。
实验方案设计如下表所示:
实 验 步 骤 | 实 验 现 象 | 实 验 结 论 | 用离子方程式解释 |
①取少量滤液,滴加适量K2CO3溶液 | 若出现白色沉淀 | 滤液中含Ca(OH)2 | Ⅰ:________________ |
若无白色沉淀 | 滤液中无Ca(OH)2 |
| |
②取少量滤液,______________________________________________ | ⅰ:若出___________ | 滤液中含Na2CO3 | Ⅱ:_______________ |
ⅱ:若无___________ | 滤液中无Na2CO3 |
|
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
①活化分子间的碰撞一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③活化分子比普通分子具有较高的能量
④化学反应的实质是原子间的重新组合
⑤化学反应的实质是旧化学键的断裂和新化学键的形成
⑥化学反应的实质是活化分子有合理取向时的有效碰撞
A.①③④⑤ B.②③⑥ C.④⑤⑥ D.②④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于丙烯(CH3—CH=CH2)的说法错误的是( )
A.丙烯分子有8个σ键,1个π键
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子存在非极性键
D.丙烯分子中最多有7个原子在同一平面上
查看答案和解析>>
科目: 来源: 题型:
【题目】通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实解释正确的是( )
选项 | 现象 | 解释 |
A | KI淀粉溶液中通入Cl2,溶液变蓝 | Cl2能与淀粉发生显色反应 |
B | 浓HNO3在光照条件下变黄 | 浓HNO3不稳定,生成有色产物能溶于浓硝酸 |
C | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 说明该溶液中含有SO |
D | 向盐酸中加入浓硫酸时产生白雾 | 说明浓硫酸具有脱水性 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水氯化钙(足量)时,氯化钙质量增加25.2g,则原混合气体中CO2的质量为( )
A.24.4gB.19.7gC.13.2gD.12.5g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com