
科目: 来源: 题型:
【题目】某校研究性学习小组选用下图装置组装制备纯净干燥的NH3并探究NH3与CuO发生的反应,同时检验和收集非固态产物。请回答下列问题:
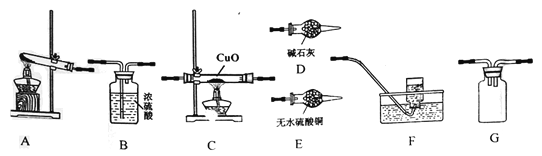
(1)完成实验所需装置按气流方向从左到右的连接顺序为___________________________。
(2)连接好装置后应首先____________________________,然后添加药品进行实验。
(3)装置A中发生反应的化学方程式为__________________________________。
(4)D中盛放碱石灰的仪器名称是________________,E装置的作用是___________________。
(5)通过进一步检测发现F中收集到的气体是一种常见的单质气体,硬质玻璃管中得到一种固体单质。试描述该小组同学还能观察到的其它现象为:___________________________;C中反应的化学方程式为:__________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,在体积为10mL、物质的量浓度为0.1mol/L的某酸HA溶液中逐滴滴入物质的量浓度为0.lmol/L的NaOH溶液,测得混合溶液的pH随NaOH溶液体积的变化如图所示(忽略混合后溶液体积的变化)。请回答以下问题:
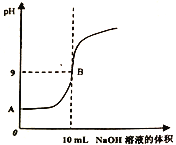
(1)HA为___________(填“强酸”或“弱酸”),做出该判断的理由是____________________。
(2)常温下,0.1mol/L NaOH溶液中由水电离出的c(OH-)=__________mol/L;B点时,溶液中由水电离出的c(OH-)=__________mol/L。
(3)B点时,混合溶液中各离子浓度的大小关系为________________________,c(HA)+ c(A-)=__________mol/L。
(4)若测得NH4A溶液的pH=7,且将HA溶液滴入(NH4)2CO3溶液中有CO2生成,则相同条件下,的物质的量浓度下列溶液的pH由小到大的顺序为___________________。
a.NH4A b.NH4Cl
c.NH4HCO3 d.(NH4)2SO4
查看答案和解析>>
科目: 来源: 题型:
【题目】不能作为判断氯、磷两种元素非金属性强弱的依据的是( )
A. 氧化性:Cl2>红磷 B. 单质沸点:红磷>Cl2
C. 氢化物稳定性:HCl>PH3 D. 酸性:HClO4>H3PO4
查看答案和解析>>
科目: 来源: 题型:
【题目】氧、硫、硒、碲等氧族元素在化合物中常表现出多种氧化态,含氧族元素的化合物在研究和生产中有许多重要用途。请回答以下问题:
(1)氧、硫、硒三元素的第一电离能由大到小的顺序为_______________________(用元素符号回答)。
(2)基态Se原子的价层电子排布式为___________,其原子核外有______________种运动状态不同的电子。
(3)气态SO3为单分子状态,其中S原子的杂化轨道类型为________。若SO3的三聚体(SO3)3的环状结构如图所示,则该结构中S原子的杂化轨道类型为____________________。
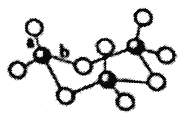
(4)氧族元素的气态氢化物中,H2S的稳定性强于H2Se,原因是________________________________。
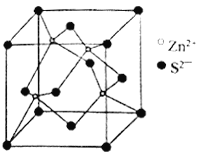
(5)氧、硫分别与钙形成两种化合物的晶格能大小为 CaO __________CaS (填“>”,“<”或“=”)。 (6)硫化锌在光导材料、涂料等行业中应用广泛,其晶体结构如图,则该晶体属于________晶体,化学式为__________,若晶体的密度为ρg·cm-3,则晶胞边长为____________cm (阿伏加德罗常数的值用NA表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关乙炔的叙述中,既不同于乙烯又不同于乙烷的是( )
A.能燃烧生成二氧化碳和水
B.能跟溴水发生加成反应
C.能跟酸性KMnO4溶液发生氧化反应
D.能与氯化氢反应生成氯乙烯
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述是不正确的是
A. 标准状况下,11.2L水所含分子数为0.5NA
B. 2.3g钠变为钠离子失去电子数为0.1NA
C. 常温常压下,2g氢气含有的原子数为2NA
D. 100 mL 2.0 mol/L的硫酸钠溶液中所含硫酸根离子数目为0.2 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸氢钠俗称小苏打,其水溶液显____________性(填“酸”、“碱”或“中”)。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为___________________。等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者____________后者(填“>”、“<”或“=”)。
(3)除去碳酸钠固体中碳酸氢钠的方法是____________(填“加热”或“溶解过滤”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验能获得成功的是
A.用溴水可以鉴别苯、CCl4、己烯
B.加浓溴水,然后过滤可除去苯中少量己烯
C.苯、溴水、铁粉混合制成溴苯
D.可用分液漏斗分离己烷和苯的混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】硼及硼的化合物有着广泛的用途。请回答下列问题:
(1)硼在元素周期表中的位置为_________,电子排布式是________,硼元素有两种天然同位素10B和11B,硼元素的近似相对原子质量为10.8,则两种同位素原子的原子个数之比为_______。
(2)单质硼(B)在一定条件下与NaOH溶液反应生成NaBO2和一种气体,请写出该反应的化学方程式________________。
(3)硼酸(H3BO3)是一种白色片状晶体,微溶于水,对人体的受伤组织有着和缓的防腐消毒作用。硼酸是一元弱酸,室温时0.1mol/L硼酸的pH为5,计算硼酸的电离常数K=__________。氟硼酸(HBF4)是一种强酸,仅以离子状态存在于水中,请写出BF4﹣的电子式__________。
(4)B2H6是硼的一种气态氢化物,因组成与乙烷(C2H6)相似而被称为乙硼烷。
①经测定B2H6中B原子最外层也满足8电子结构,由此推测B2H6与C2H6分子结构_________(填“相同”或“不相同”)。
②B2H6可由BF3与NaBH4在一定条件下反应制得,写出该反应的化学方程式_________。
③B2H6是强还原剂,它与水反应生成H3BO3和H2。若有0.1mol B2H6与水完全反应,则产生H2在标准状况下的体积为_________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com