
科目: 来源: 题型:
【题目】常温下,用0.1000mol/L的盐酸滴定20.00mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是( )
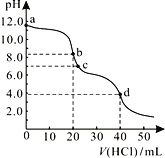
A. c点处的溶液中c(Na+)-c(Cl-)=c(HCO![]() )+2c(CO
)+2c(CO![]() )
)
B. a点溶液呈碱性的原因用离子方程式表示为: CO![]() +2H2O
+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
C. b点溶液中c(Na+)> c(HCO![]() )> c(Cl-)
)> c(Cl-)
D. d点处溶液中水的电离程度大于b点处
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:NH4++OH-![]() NH3↑+H2O,有一瓶澄清的溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl-中的几种,取该溶液进行如下实验:
NH3↑+H2O,有一瓶澄清的溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl-中的几种,取该溶液进行如下实验:
(1)填表(在表中的空白处填写离子符号)
步骤 | 实验步骤 | 肯定不存在的离子 |
① | 用pH试纸测得该溶液呈酸性 | ________________ |
② | 另取l0mL该溶液逐滴加入稀NaOH溶液,使溶液从酸性逐渐变为碱性,此过程中无沉淀生成 | ________________ |
③ | 向②所得的溶液中加入足量Na2CO3溶液,过滤、洗涤、干燥,得到1.97g白色固体 | ________________ |
④ | 另取l0mL该溶液,加入浓NaOH溶液并加热,收集到224mL气体A(标准状况下) | |
⑤ | 另取l0mL该溶液,加入足量稀硝酸和AgNO3溶液,产生2.87g白色沉淀 |
(2)根据以上事实,在上述离子中,该溶液肯定存在的离子有________________。
(3)气体A溶于水可配成溶液A (该溶液的密度比水小),把50g浓度为c1的浓A溶液(溶质质量分数为ω1)与V mL水混合,得到浓度为c2的稀A溶液(溶质质量分数为ω2)。若ω1=2ω2,则:
①c1_____c2,②V_________50mL(填“>”“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中,正确的是
A. 在一个基态多电子的原子中,可以有两个运动状态完全相同的电子
B. 在一个基态多电子的原子中,不可能有两个能量完全相同的电子
C. 在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高
D. 某基态原子错误的核外电子排布图为![]() 该排布图违背了泡利原理
该排布图违背了泡利原理
查看答案和解析>>
科目: 来源: 题型:
【题目】淀粉、淀粉酶、基因(DNA片段)的基本单体依次是( )
A. 葡萄糖、蛋白质、DNA B. 蔗糖、氨基酸、核糖核苷糖
C. 葡萄糖、氨基酸、脱氧核苷酸 D. 麦芽糖、多肽、核苷糖
查看答案和解析>>
科目: 来源: 题型:
【题目】双氧水(主要成分H2O2)不仅是常见的氧化剂、还原剂,而且能和N2H4反应生成氮气和水,因此广泛应用于火箭推进器中。
(1)H2O2的电子式为________,其中氧的化合价为_________。
(2)如图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式________。
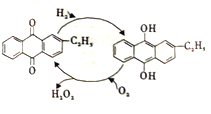
(3)为了除去酸性溶液中的Fe2+,常常要加入双氧水,写出相应离子方程式_____,用3%的双氧水清洗伤口,会有大量气泡产生,其可能的原因是_____________。
(4)H2O2可看作二元酸,写出它在水中第一步电离的方程式_____;它与足量Ba(OH)2反应的化学方程式为___________。
(5)Mg-H2O2以酸性电池采用海水作电解质溶液(加入一定量的释硫酸),该电他的负极材料是_____,正极的反应式为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某物质X 能发生如图转化(四种物质均含元素R ) ,回答下列问题:
![]()
Ⅰ.已知X是一种能使湿润的红色石蕊试纸变蓝的气体,与A化合生成一种正盐,则:
(1)X的电子式为______,写出X与Z在催化剂作用下生成两种无毒物质的化学方程式_____。
(2)在含Cu2+离子溶液中,RO2-离子可转化为RO,写出Cu+和RO2-离子在酸性水溶液中反应的离子方程式___________。
Ⅱ.若X的产量是衡量一个国家石油化工水平的标志,且Y与A在浓硫酸作用下生成一种具有香味的物质B, 则:
(1)X的分子式为________,①的反应类型是_______,工业上以X为为原料可以合成一种生活中最常见的有机高分子材料,其反应的化学方程式为__________。
(2)实验室利用Y与A制备B,写出化学反应方程式:________,实验中配制一定比例的Y、A和浓硫酸的混合液的方法(加入试剂的顺序)是:_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应最终无沉淀产生的是
A. NaHCO3溶液中滴加Ba(OH)2溶液
B. Na2SiO3溶液中通入过量 CO2
C. 久置Na2SO3溶液滴加过量的盐酸酸化的BaC12溶液
D. NaAlO2溶液中滴加过量盐酸
查看答案和解析>>
科目: 来源: 题型:
【题目】关于乙炔的说法错误的是
A. 乙炔的键角为180°,是非极性分子
B. 碳原子sp杂化轨道形成σ键、未杂化的两个2p轨道形成两个π键,且互相垂直
C. 碳碳三键中三条键能量大小相同,其键长是碳碳单键的![]()
D. 乙炔分子中既有极性键也有非极性键
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如下图所示:
X | Y | |
Z | W |
请回答下列问题:
(1)W位于周期表中第________周期,第______族;
(2)X可形成双原子分子,其分子的电子式是_________;Y和氢元素形成的10电子微粒中常见+1价阳离子为_______(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子的水解方程式__________。
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式_________________________。
(4)将0.20molYZ2和0.10molO2充入一个固定容积为5L的密闭容器中,在一定温度并有催化剂存在下,进行反应,经半分钟达到平衡,测得溶液中含YZ30.18mol,则v(O2)=________mol/(L·min);若温度不变,继续通入0.20molYZ2和0.10molO2,则平衡_______移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol<n(YZ3)<_______mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应都有水参加,其中属于氧化还原反应,而水既不做氧化剂,又不做还原剂的是
A.2F2+2H2O=4HF+O2 B.2Na+2H2O=2NaOH+H2↑
C.C12+H2O=HC1O+HC1 D.C+H2O![]() CO+H2
CO+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com