
科目: 来源: 题型:
【题目】化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:
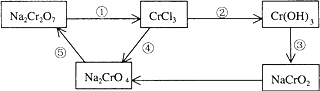
(l)在上述有编号的步骤中,需用还原剂的是_______,需用氧化剂的是___________ (填编号)。
在上述循环中,既能与强酸反应又能与强碱反应的两性物质是______(填化学式)。
(3)完成并配平步骤①的化学方程式,并用单线桥法标出电子转移的方向和数目:_______。
□Na2Cr2O7+□KI+□HCl→□CrCl3+□NaCl+□KCl+□I2+□
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. SO2和SO3都是酸性氧化物,二者的水溶液都是强酸
B. 将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化
C. 硫粉在适量的纯氧中燃烧可以生成大量的SO3
D. 富含硫磺的矿物在工业上可用于制造硫酸
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A、B、C、D在周期表中位置如图所示,其中元素D原子最外层有3个电子。请用相应的化学用语回答:
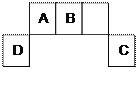
(1)A与氢元素可以形成很多化合物,在这些化合物中都含有_________(选填“共价”或“离子”)键;与C相邻且最外层电子比C少1个的离子结构示意图为 _________________。B在元素周期表中位于____________________。B、C、D形成的离子的半径由大到小依次为 _________________。(填相应的离子符号)
(2)元素A形成的最简单氢化物和氧气在KOH溶液中可构成燃料电池,该电池工作时正极的电极反应式为 ___________________________________。
(3)D的最高价氧化物的水化物与NaOH反应的化学方程式是:
________________________________________。
(4)由A与S形成的液态化合物AS2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215 kJ。 该反应的热化学方程式为_________________________________。
(5)已知298K时,Fe(s) + ![]() O2(g) == FeO(s) ; ΔH= -272.0 kJ · mol-1
O2(g) == FeO(s) ; ΔH= -272.0 kJ · mol-1
2D(s) + ![]() O2(g) == D2O3(s) ; ΔH= -1675.7 kJ · mol-1
O2(g) == D2O3(s) ; ΔH= -1675.7 kJ · mol-1
写出D单质和FeO反应的热化学方程式是_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
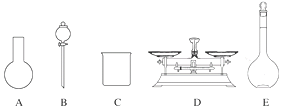
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)装置A中仪器①的名称是__________,装置B中仪器②的名称是__________, 装置D中仪器③的名称是___________。
(2) 从碳酸钙和氯化钠固体混合物中得到纯净氯化钠固体,应选择装置___________(填代表装置图的字母,下同);从海水中获得淡水可选择装置____________;从碘水中分离出I2,应选择装置___________,该分离方法的名称为_________________。
(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Fe3+、Cl-离子。可用________方法除去。
查看答案和解析>>
科目: 来源: 题型:
【题目】有BaCl2和NaCl的混合溶液a L,将它均分成两份.一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl﹣完全沉淀.反应中消耗 x mol H2SO4、y mol AgNO3.据此得知原混合溶液中的c(Na+)为( )
A. ![]() mol/L B.
mol/L B. ![]() mol/L C.
mol/L C. ![]() mol/L D.
mol/L D. ![]() mol/L
mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气是人类未来最理想的燃料,以水为原料大量制取氢气的最理想的途径是
A.利用太阳能直接使水分解产生氢气
B.以焦炭和水制取水煤气(含CO和H2)后分离出氢气
C.用铁和盐酸反应放出氢气
D.由热电站提供电力电解水产生氢气
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:N2(g)+3H2(g) 2NH3(g)△H=﹣192kJmol﹣1.向 M、N 中,都通入 xmol N2 和ymol H2的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是 ( )

A. 若x:y=1;2,则平衡时,M中的转化率:N2>H2
B. 若x:y=1:3,当M中放出热量172.8kJ时,N2的转化率为90%
C. 若x=1,y=3,则达到平衡时反应物的转化率N>M
D. 平衡时N2气体在两容器中体积分数可能相等
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
84消毒液
有效成分 NaClO
规格 1 000 ml
质量分数 25%
密度 1.19 g·cm-3
(1)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=____mol·L-1。
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL该消毒液。下列说法正确的是________(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
(3)配制溶液的过程如下,该同学的错误步骤有(____)
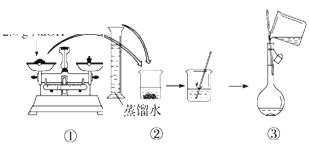
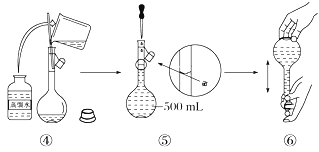
A.1处 B.2处 C.3处 D.4处
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。需用浓硫酸的体积为____mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com