
科目: 来源: 题型:
【题目】氧可与多种元素形成化合物,设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A. 7.2 g CaO2晶体中阴离子数目为0.2NA
B. 4.0 g H![]() O中所含电子数为2NA
O中所含电子数为2NA
C. 6.2 g Na2O溶于100 mL水中所得溶液的物质的量浓度为2 mol·L-1
D. 标准状况下,将22.4 L Cl2通入足量水中发生反应,转移电子的数目为NA
查看答案和解析>>
科目: 来源: 题型:
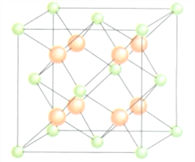
【题目】已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如图。
请回答下列问题:
(1)A元素的名称是_____________________;
(2)B的元素符号是___________________,C的元素符号是______________,B与A形成的化合物比C与A形成的化合物沸点高,其原因是_________________________
(3)E位于元素周期表中第_________周期,第_________族的元素,其元素名称是_________________,它的+2价离子的电子排布式为__________________
(4)从图中可以看出,D跟B形成的离子化合物的化学式为____________;该离子化合物晶体的密度为ag·cm-3,则晶胞的体积是______________________只求要求列出算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下面是s能级与p能级的原子轨道图:

请回答下列问题:
s电子的原子轨道呈________形,每个s能级有_______个原子轨道;
p电子的原子轨道呈________形,每个p能级有_______个原子轨道。
(2)写出下列元素基态原子的电子排布式:
①Co___________________________;②Cu_____________________________。
(3)画出下列元素原子的轨道表示式(电子排布图):
①N______________________________;②F_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-===2Fe2++I2+3H2O
B. 0.1 mol·L-1 NH4Al(SO4)2溶液与0.2 mol·L-1 Ba(OH)2溶液等体积混合:Al3++2SO![]() +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO![]() +2H2O
+2H2O
C. 向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-===A2-+H2O
D. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O===HClO+HSO![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是( )
A.2-甲基丁烷也称异丁烷
B.同系物的化学性质基本相似
C.常温下乙酸乙酯在水中的溶解度小于乙醇在水中的溶解度
D.苯与浓硝酸、浓硫酸共热并保持50~60 ℃反应生成硝基苯
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中含有的离子可能是K+、Ba2+、Al3+、Mg2+、AlO![]() 、CO
、CO![]() 、SiO
、SiO![]() 、Cl-中的几种,现进行如下实验:
、Cl-中的几种,现进行如下实验:
①取少量溶液加氢氧化钠溶液过程中无沉淀生成
②另取少量原溶液,逐滴加入5 mL 0.2 mol·L-1盐酸,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失。
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到白色沉淀。
下列说法中正确的是( )
A. 该溶液中一定不含Ba2+、Mg2+、Al3+、SiO![]() 、Cl-
、Cl-
B. 该溶液中一定含有K+、AlO![]() 、CO
、CO![]() 、Cl-
、Cl-
C. 该溶液是否有K+需做焰色反应(透过蓝色钴玻璃片)
D. 可能含有Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
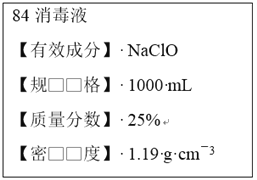
(1)该“84消毒液”的物质的量浓度约为________mol·L-1。
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=________mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是________(填序号)。

A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
Ⅱ.向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式_________________________________________
(2)下列三种情况下,离子方程式与(1)相同的是____________(填序号).
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图1中的_________曲线表示(填序号).
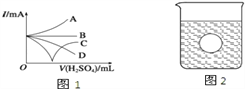
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图2所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应.在此实验过程中,小球将____________.
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO![]() 、SO
、SO![]() 、Cl﹣中的若干种离子.该小组同学取100mL水样进行实验,向水样中先滴加硝酸钡溶液,再滴加1mol/L的硝酸,实验过程中沉淀质量的变化情况如下图所示:(提示:Al3+与CO
、Cl﹣中的若干种离子.该小组同学取100mL水样进行实验,向水样中先滴加硝酸钡溶液,再滴加1mol/L的硝酸,实验过程中沉淀质量的变化情况如下图所示:(提示:Al3+与CO![]() 不共存)
不共存)
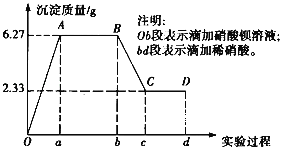
(1)水样中一定含有的阴离子是_____,其物质的量浓度之比为_____.
(2)写出BC段所表示反应的离子方程式:_____.
(3)由B到C点变化过程中消耗硝酸的体积为_____.
(4)试根据实验结果推测K+是否存在?_____(填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是_____.(若K+不存在,则不必回答该问).
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关SO3的说法中正确的是( )
A. 标准状况下,1molSO3的体积约为22.4L
B. SO3极易溶于水,且与水反应生成H2SO4
C. 将SO3加入BaCl2溶液无明显现象
D. SO2和SO3均具有漂白性,能使紫色石蕊溶液褪色
查看答案和解析>>
科目: 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 molPCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是( )
A. 反应在前50 s的平均速率为v(PCl3)=0.0032 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol·L-1,则反应的△H<0
C. 相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com