
科目: 来源: 题型:
【题目】具有下列性质的有机化合物中同分异构体数目最多的是(不考虑立体异构)( )
选项 | A | B | C | D |
分子式 | C4H8Cl2 | C5H10O2 | C4H8O2 | C9H12 |
类别 | 含氯化合物 | 羧酸 | 酯 | 含有苯环的烃 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 反应N2 (g) +3H2 (g) ![]() 2NH3 (g)的ΔH < 0,ΔS >0
2NH3 (g)的ΔH < 0,ΔS >0
B. 地下钢铁管道用导线连接锌块可以减缓管道的腐蚀
C. 常温下,Ksp[Mg(OH)2]=5.6×10-12,pH=10的含Mg2+溶液中,c(Mg2+ )≤5.6×10-4 mol·L-1
D. 常温常压下,锌与稀H2SO4反应生成11.2 L H2,反应中转移的电子数为6.02×1023
查看答案和解析>>
科目: 来源: 题型:
【题目】已知下列十种物质:
①H2O ②Cu ③NO ④SiO2 ⑤稀硫酸 ⑥氢氧化钡 ⑦饱和FeCl3溶液 ⑧氨水 ⑨稀硝酸 ⑩硫酸铝
根据上述提供的物质,回答下列问题:
(1)属于纯净物的是__________,属于电解质的是__________。(填数字序号)
(2)发生中和反应的离子方程式为H++OH-===H2O,该离子反应对应的化学方程式有__________________________________。
(3)实验室制备少量Fe(OH)3胶体所用到的物质有________(填数字序号),发生反应的离子方程式为_________________________。
(4)实验室配制0.5 mol·L-1 245 mL⑩的溶液,需要用到的玻璃仪器有玻璃棒、烧杯、胶头滴管、________,需要用托盘天平称取溶质的质量为________g,从配制好的溶液中取出100 mL,其中含有的SO42—数目为________(设NA为阿伏加德罗常数的值)。
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌于一体的新型高效多功能水处理剂,干燥的高铁酸钾在198 ℃以下是稳定的,受热易分解。高铁酸钾在水处理过程中涉及的变化过程有
①蛋白质的变性 ②蛋白质的盐析 ③胶体聚沉 ④盐类水解 ⑤焰色反应 ⑥氧化还原反应
A. ①②③④ B. ①③④⑥
C. ②③④⑤ D. ②③⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系,下列有关物质的推断不正确的是( )
![]()
A. 若甲为AlCl3,则丁可能是NaOH B. 若甲为N2,则丁可能是O2
C. 若甲为Fe,则丁可能是硝酸 D. 若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有机化学反应方程式及反应类型均正确的是( )
选项 | 化学反应方程式 | 反应类型 |
A | CH3COOH+CH3CH2OH | 取代反应 |
B | CH4+Cl2 | 置换反应 |
C | CH3CH=CH2+Br2 CH2BrCH2CH2Br | 加成反应 |
D |
| 取代反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】尼龙-66是一种重要的合成纤维,它是由己二酸和己二胺[H2N—(CH2)6-NH2]以相等的物质的量在一定条件下聚合而成的,下列叙述中不正确的是( )
A. 尼龙-66的结构简式是
B. 合成尼龙-66的反应属于缩聚反应
C. 合成尼龙-66的反应基础是酯化反应
D. 尼龙-66的长链结构中含有肽键
查看答案和解析>>
科目: 来源: 题型:
【题目】金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍。下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
A. 电解后,电解槽底部的阳极泥中只有金属Pt
B. 电解过程中,电解质溶液的质量可能保持不变
C. 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D. 阳极发生氧化反应,其电极反应式:Ni2++2e-![]() Ni
Ni
查看答案和解析>>
科目: 来源: 题型:
【题目】温度为T1时,在三个容积均为1 L的恒容密闭容器中仅发生反应:2NO2(g)![]() 2NO(g)+O2 (g) (正反应吸热)。实验测得: v正= v(NO2)消耗=k正c2(NO2 ),v逆= v(NO)消耗=2v(O2)消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。下列说法正确的是
2NO(g)+O2 (g) (正反应吸热)。实验测得: v正= v(NO2)消耗=k正c2(NO2 ),v逆= v(NO)消耗=2v(O2)消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。下列说法正确的是
容器编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
I | 0.6 | 0 | 0 | 0.2 |
II | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A. 达平衡时,容器I与容器Ⅱ中的总压强之比为 4∶5
B. 达平衡时,容器中Ⅱ中 c(O2)/ c(NO2) 比容器I中的大
C. 达平衡时,容器Ⅲ中NO的体积分数小于50%
D. 当温度改变为 T2时,若 k正=k逆,则 T2<T1
查看答案和解析>>
科目: 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是( )
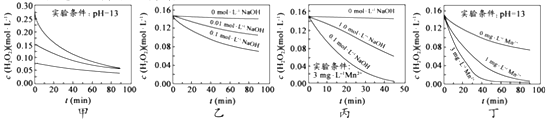
A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液PH 越小,H2O2分解速率越快
C. 图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com