
科目: 来源: 题型:
【题目】关于电解NaCl水溶液,下列叙述正确的是 ( )
A. 电解时在阳极得到氯气,在阴极得到金属钠
B. 若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
C. 若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
D. 电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
查看答案和解析>>
科目: 来源: 题型:
【题目】用KMnO4氧化质量分数为36.5%的盐酸,反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
(1)若此盐酸的密度为1.2g/cm3,其物质的量浓度为__________________。
(2)此反应中氧化剂与还原剂的物质的量的比为________________。
(3)若15.8g KMnO4完全反应,产生标准状况下Cl2的体积为______,若改用MnO2代替15.8g KMnO4制Cl2 (MnO2被还原为MnC12).产生相同体积的Cl2时需要MnO2的物质的量为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、NH4+、Ba2+、Fe3+、C1-、SO42-、CO32-,将该混合物溶于水后得澄清溶液,现取3份100 mL该溶液分别进行如下实验:
序号 | 实验内容 | 实验结果 |
1 | 加过量盐酸 | 无气体产生 |
2 | 加足量NaOH溶液并加热 | 收集到气体2.24 L(标准状况),并有红褐色沉淀生成,将沉淀过滤洗涤、干燥、灼烧至质量不再变化,称重得1.60 g固体。 |
3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量 | 称量读数为2.33g |
试确定溶液中一定存在的离子及其物质的量浓度(可不填满):
离子符号 | 物质的量浓度(mol·L-1) |
_____ | _____ |
_____ | _____ |
_____ | _____ |
_____ | _____ |
查看答案和解析>>
科目: 来源: 题型:
【题目】由氮的化合物引起的环境污染称为氮污染。
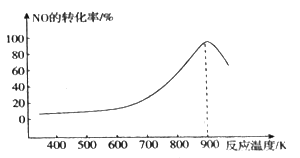
(1)己知CO将NO转化为N2的方程式为2CO(g)+2NO(g)![]() N2(g)+2CO2(g) ΔH,某研究小组在实验中研究温度对NO转化率的影响并绘制图像。
N2(g)+2CO2(g) ΔH,某研究小组在实验中研究温度对NO转化率的影响并绘制图像。
①当n(NO)/n(CO)=l,容器容积恒定时,在不同温度下反应相同的时间测得NO的转化率变化如图所示,则在此反应时间内应控制反应的最佳温度在______左右,该反应的ΔH_____0 (填>或<)。
②该反应的平衡常数表达式为K=__________。
要同时提高平衡常数的值和NO的平衡转化率,可采取的措施是________。
A.降低温度 B.及时将CO2和N2从反应体系中移走
C.升高温度 D.增大压强
③在恒温恒容容器中按体积比2∶1充入CO和NO的混合气体,下列选项能说明正反应速率大于逆反应速率的是_____________(填序号)。
A.CO的浓度保持恒定 B.混合气体的平均相对分子质量逐渐减小
C.CO和NO的物质的量之比逐渐增大 D.CO、NO、N2的速率之比为2∶2∶1
(2)在催化剂存在的条件下,用H2可以将NO还原为N2,己知:

则氢气和一氧化氮反应生成氮气和水蒸气的热化学方程式是_________________。
(3)MAP沉淀法是一种比较新颖有效的处理氨氮废水的方法,.原理如下:向含NH4+的废水中投加磷酸盐和镁盐,使之和NH4+生成难溶复盐MgNH4PO4·6H2O (简称MAP)。MAP沉淀法需要控制反应的PH在7.5-10之间,当PH过高时不利于生成MAP的原因是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某酯A,其分子式C6H12O2,已知
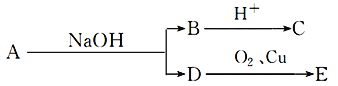
又知B、C、D、E均为有机物,D不与Na2CO3溶液反应,E不能发生银镜反应,则A结构可能有( )
A. 5种 B. 4种 C. 3种 D. 2种
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)溶质的质量分数为b%的KOH溶液,经加热蒸发去ag水后,质量分数变成 2b%,体积为VmL,则此时溶液的物质的量浓度为___________。(答案必须为最简形式)
(2)将6mol/L的盐酸(ρ=1.19g/cm3)50mL稀释成3mol/L的盐酸(ρ=1.10g/cm3),需加水的体积为__________mL。
(3)密度为1.19g/cm3的盐酸,质量分数为25%。该盐酸用等体积的水稀释后,所得溶液中溶质的质量分数_______(填“大于”、“小于”或“等于”)12.5%。
(4)已知20℃时,饱和NaCl溶液的密度为ρg/cm3,物质的量浓度为c mol/L,则饱和NaCl溶液的溶解度为_________g。(答案必须为最简形式)
(5)相同质量的NO2和N2O4的质子数之比为_______,电子数之比为_______________。
(6)请用单线桥表示化学方程式CaH2+2H2O=Ca(OH)2+2H2↑电子转移的方向和数目___________。
(7)若将过量的NaOH溶液加入NH4HCO3溶液中,则反应的化学方程式__________________,若将NaOH溶液加入过量的NH4HCO3溶液中,则反应的离子方程式为__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积。图中E为量气装置。

本实验可供选用的药品还有:稀硫酸、稀盐酸、过氧化钠、大理石、水。
己知:2 Na2O2+2H2O=4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2 试回答:
(1)图中装置的连接顺序是(填装置的字母编号),其中连接胶管及支持装置均省略:_________。
(2)装置C中放入的反应物是________和_________________。(写化学式)
(3)装置A的作用是__________________;装置B的作用是_____________________________。
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,应注意_____________________________。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数。
c.读数时应上下移动乙管,使甲、乙两管液面相平。
d.读数时不一定使甲、乙两管液面相平。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式表达正确的是
A. 泡沫灭火器的灭火原理:2A13+ +3 CO32-+3H2O= 2Al(OH)3↓+ 3CO2↑
B. 小苏打溶液呈碱性的原因:HCO3-+H2O![]() H3O++ CO32-
H3O++ CO32-
C. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O
D. 向硫酸铝铵溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3·H2O+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于苯的说法中正确的是( )
A. 苯分子中的所有化学键都完全相同
B. 苯分子中含有碳碳双键,能使酸性高锰酸钾溶液褪色
C. 苯是一种密度比水小,不溶于水的有特殊气味的无色液体
D. 在催化剂存在下,苯能与溴水发生取代反应,生成溴苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com