
科目: 来源: 题型:
【题目】NO2通过盛有水的洗气瓶,转移0.03mol电子时,参加反应的NO2气体在标准状况下的体积为
A. 224mL B. 336mL C. 448mL D. 1008mL
查看答案和解析>>
科目: 来源: 题型:
【题目】丁香醛是常用的一种食用香精。存在下列转化关系:
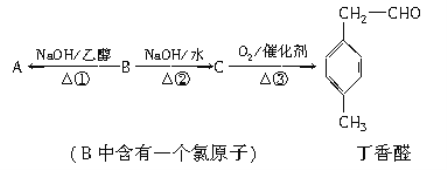
(1)B的分子式为________,C中含氧官能团的名称为________。
(2)反应②的化学方程式为____________________________________。
(3)A发生加聚反应所得产物的结构简式为________________。
(4)与A含有相同官能团的芳香族化合物的同分异构体还有________种(不考虑顺反异构),其中只有一个取代基且不含甲基的物质的结构简式为________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是__________,KMnO4发生_______反应,被氧化的元素是__________,氧化产物是___________,若有1mol KMnO4参加反应时,该反应转移电子的个数是_______;若反应生成11.2LCl2(标准状况)则被氧化的氯化氢为_________mol, 请在下面方程式中用“双线桥法”表示该反应中电子转移的方向和数目__________________________。
2KMnO4 + 16HCl ![]() 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,发生下列几种反应:①16H++10Z-+2XO![]() ===2X2++5Z2+8H2O ②2A2++B2===2A3++2B③2B-+Z2===B2+2Z-根据上述反应,判断下列结论错误的是
===2X2++5Z2+8H2O ②2A2++B2===2A3++2B③2B-+Z2===B2+2Z-根据上述反应,判断下列结论错误的是
A. 溶液中可发生:Z2+2A2+===2A3++2Z-
B. 氧化性强弱的顺序为:XO![]() >Z2>B2>A3+
>Z2>B2>A3+
C. Z2在①③反应中为还原剂
D. X2+是XO![]() 的还原产物
的还原产物
查看答案和解析>>
科目: 来源: 题型:
【题目】下列除去杂质(括号内物质为少量杂质)的方法中,正确的是( )
A. 乙烷(乙烯):光照条件下通入Cl2,气液分离
B. 乙酸乙酯(乙酸):用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏
C. CO2(SO2):气体通过盛氢氧化钠溶液的洗气瓶
D. 乙醇(乙酸):加足量浓硫酸,蒸馏
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸(HNO2)在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,其还原产物可能是
①NO ②NO2 ③HNO3 ④N2 ⑤NH3
A.①③ B.①②④ C.①④⑤ D.全部
查看答案和解析>>
科目: 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5
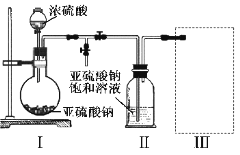
(1)装置I中产生气体的化学方程式为__________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是_________。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。

实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸
d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是____________。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________________g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测得结果____(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com