
科目: 来源: 题型:
【题目】PFS是水处理中重要的絮凝剂,下图是以回收的废铁屑为原料制备PFS的一种工艺流程。
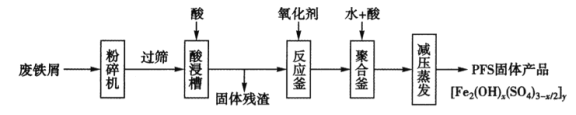
(1)酸浸槽以及聚合釜中用到的酸应是__________;PFS中铁元素的化合价为__________;在酸浸槽中,为了提高浸出率,可以采取的措施有_________(写两条)。
(2)若废铁属含有较多铁锈(Fe2O3·xH2O),则酸浸时反应的化学方程式有_____________。
(3)如果反应釜中用H2O2作氧化剂,则反应的离子方程式为________;生产过程中,发现反应釜中产生了大量的气体,且温度明显升高,其原因可能是___________。
(4)聚合釜中溶液的pH必须控制在一定的范围内。如果溶液酸性过强,造成的后果是________。如果溶液酸性太弱又会生成大量的氢氧化铁沉淀。若溶液中Fe3+的浓度为1mol·L-1,当Fe3+开始沉淀时,涪液的pH约为_________。[已知Fe(OH)3的Ksp≈1.0×10-39]。
查看答案和解析>>
科目: 来源: 题型:
【题目】将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L(标况)CO2和3.6g水,对于组成判断正确的是
A. 可能是甲烷和乙烷的混合气体 B. 一定是甲烷和乙烯的混合气体
C. 混合气体中一定没有甲烷 D. 混合气体中一定没有乙烷
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁电池具有比能量高、无污染的特点,用下图模拟其工作原理(放电时两电极均有稳定的金属氢氧化物生成),下列有关说法中正确的是

A. 充电时,阳极上的电极反应式为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O
B. 放电时,负极上的电极反应式为:Zn-2e-+2H2O=Zn(OH)2+2H+
C. 放电时,电子由正极通过外电路流向负极
D. 充电时,阴极区溶液的pH减小
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)按如图所示操作,充分反应后:
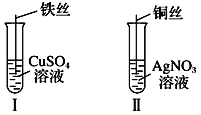
①Ⅰ中发生反应的离子方程式为______________________________________;
②Ⅱ中铜丝上观察到的现象是________________________________________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为___________。
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应物中还原产物是___________;若反应中转移了0.3 mol电子,则氧化产物的质量是___________g。
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=== 2Fe3++2Cl-,这个事实说明FeBr2的溶液中具有还原性粒子的还原性强弱为___________。
(4)黑火药爆炸时发生反应:2KNO3+S+3C=K2S+N2↑+3CO2↑,2mol KNO3氧化碳的物质的量为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】配制一定物质的量浓度的稀盐酸,结果偏高的是
A. 在容量瓶中定容时,俯视刻度线
B. 用量筒量取浓盐酸时,俯视刻度线
C. 转移溶液后,未洗涤烧杯和玻璃棒就直接定容
D. 定容后把容量瓶倒置摇匀,发现液面低于刻度线又加水至刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】砷化稼(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]_______________。
(2)根据元素周期律,元素的电负性Ga______(填“大于”或“小于”, 下同)As,第一电离能B ____ Ga;BF3和NH3的分子能够通过配位键相结合的原因是_______。
(3)杀虫剂Na3AsO4中阴离子的空问构型为______,As原子采取________杂化。
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是____________。
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价健数为______;A原子距离B原子所在六面体的侧面的最短距离为______ (用x表示)pm ;该晶胞的密度为_____g·cm-3。(阿伏伽德罗常数用NA表示)。

查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于物质的量浓度表述正确的是
A. 0.2mol/L Na2SO4溶液中含有Na+和SO42-总物质的量为0.6mol
B. 用1L水吸收22.4L氯化氢(标况下)所得盐酸的浓度是1mol/L
C. 10g 98%的硫酸(密度为1.84g·cm-3)与10mL 18.4mol/L 的硫酸的浓度相同
D. 50mL 2mol/L NaCl溶液和100 mL 0.5mol/L MgCl2溶液中,Cl-物质的量浓度相等
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在一定条件下,反应 X(g)+3Y(g![]() 2Z(g) △H=-a kJ/mol(a>0 ),某实验小组测得X的转化率(α)在不同温度与压强(P)下 的实验数据,三者之间关系如下图所示。下列说法正确的是
2Z(g) △H=-a kJ/mol(a>0 ),某实验小组测得X的转化率(α)在不同温度与压强(P)下 的实验数据,三者之间关系如下图所示。下列说法正确的是

A. 图中a、b两点对应的平衡常数相等
B. 上述反应在达到平衡后,缩小体积,Y的转化率提高
C. 升高温度,正、逆反应速率增大,平衡向正反应方向移动
D. 将2.0molX、6.0molY,置于密闭容器中发生反应,放出的热量为2akJ
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质的分离说法正确的是
A. 检查是否漏水是滴定管、容量瓶、分液漏斗等仪器使用的第一步操作
B. 碘水中加CCl4振荡静置后,上层为紫色,下层几乎为无色
C. 可用加热法分离NH4Cl(s)和I2(s)
D. 蒸馏、分馏和干馏都是利用组分沸点不同而分离的方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com