
科目: 来源: 题型:
【题目】某工业残渣主要成分为Fe2O3(含有少量FeO、Cu、Mg等杂质)。某课外兴趣小组利用该残渣制取Fe2O3粉末的流程如下:(说明:流程中“向黄色溶液加入MgO”的目的是调节溶液的酸碱性,使Fe3+生成沉淀而Mg2+不沉淀。)
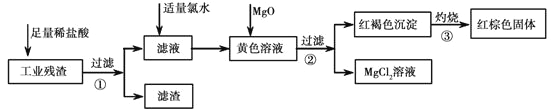
请回答下列问题:
(1)加入足量稀盐酸后,发生化学反应的类型有_____________(填写代号)。
A. 氧化还原反应 B.化合反应 C.分解反应 D.复分解反应
(2)加入适量氯水的作用是____________________________.
(3)写出灼烧红褐色沉淀时发生反应的化学方程式_____________________。实验室灼烧红褐色沉淀可选用的装置是__________(填序号)。

(4)若向黄色溶液中加入过滤①后的滤渣,发生反应的离子方程式为___________。
(5)检验黄色溶液中Fe3+是否完全沉淀的方法是:取过滤②后的少量滤液于试管中,____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】NaN3+KNO3→N2↑+K2O+Na2O此方程式是汽车剧烈碰撞时,安全气囊中发生的反应。对上述反应的描述错误的是( )
A. NaN3是还原剂,KNO3是氧化剂
B. 该反应中有一种元素的化合价发生变化
C. 若生成8 mol N2,则转移电子的物质的量为5 mol
D. 配平后物质的系数依次为10、2、1、5、16
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各离子方程式中,属于水解反应的是( )
A.HS-+H2OH2S+OH-B.HCO3-+H2OH3O++CO32-
C.HCO3-+OH-═CO32-+H2OD.NH3+H2OOH-+NH4+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液一定呈中性的是( )
A.使石蕊试液呈红色的溶液B. c(H+)=c(OH-)=10-6molL-1溶液
C.pH=7的溶液D.由强酸与强碱等物质的量反应得到的溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A是一种常见的非金属单质,B是氧化物,E是A的氢化物,D是A的最高价氧化物对应的水化物,上述物质间转化关系如图所示。下列说法错误的是 ( )

A. 若E、D的水溶液均呈酸性,则A为硫
B. 若D是一种难溶于水的物质,则A为硅
C. 若E、D的水溶液均呈酸性,则B能与水反应
D. 若D是一种难溶于水的物质,则B能与水反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1moI/L的是
A. 将6.2gNa2O溶解于水,并配成200mL溶液
B. 1L含1mol K+的K2SO4溶液
C. 将22.4LHC1溶于1L水
D. 将40.0 g NaOH溶于1L水
查看答案和解析>>
科目: 来源: 题型:
【题目】碳和氮、硫是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,SO2会形成酸雨,目前,这些有毒有害气体的处理成为科学研究的重要内容。
(1)已知热化学方程式:
①2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H1
②C(s)+ O2(g)=CO2(g) △H2
③H2(g)+ ![]() O2(g)=H2O(l) △H3
O2(g)=H2O(l) △H3
则反应④2C(s)+H2(g)=C2H2(g)的△H 为_________________________。(用含△H1、△H2、△H3关系式表示)
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)![]() N2+CO2(g) △H<0。在Tl℃时,反应进行到不同时间测得各物质的浓度(单位:mol/L)如下:
N2+CO2(g) △H<0。在Tl℃时,反应进行到不同时间测得各物质的浓度(单位:mol/L)如下:
0 | 10 | 20 | 30 | 40 | 50 | |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①1020min内,NO的平均反应速率v(NO)=___________,
②30min后,只改变某-条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是________(填字母编号)。
a.通入一定量的NO b.加入一定量的c
c.适当升高反应体系的温度 d.加入合适的催化剂
e.适当缩小容器的体积
③若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c(NO)
=_________ml/L。NO的转化率______(填“增大”“减小”或“不变”)。
④下列说法中可以说明该反应已达到平衡状态的是_________。
a.体系内混合气体的密度保持不变 b.NO、N2、CO2、的物质的量之比为2∶1∶1
c.容器内气体的总压强保持不变 d. NO体积分数不再改变
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:____________________;
②当甲中消耗2.24LO2(标准状况)时,乙中________ (填“a”或“b”)增重________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于强弱电解质及非电解质的组合完全正确的是( )
A | B | C | D | |
强电解质 | NaCl | H2SO4 | CaCO3 | HNO3 |
弱电解质 | HF | BaSO4 | HClO | CH3COOH |
非电解质 | Cl2 | CO2 | H2S | SO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 向Ba(OH)2溶液中滴加稀硫酸:OH-+H+==H2O
B. 向FeCl2溶液中通入氯气:Fe2++Cl2-=Fe3++2Cl-
C. 将NaHCO3溶液与H2SO4溶液混合:HCO3-+H+=H2O+CO2↑
D. 用醋酸除水垢:2H++Ca2++CO32-==Ca2++CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com