
科目: 来源: 题型:
【题目】【加试题】二氧化碳是一种宝贵的碳氧资源。以CO2和NH3为原料合成尿素是固定和利用CO2
的成功范例。在尿素合成塔中的主要反应可表示如下:
反应 I:2NH3(g)+CO2(g) ![]() NH2COONH4(s) ΔH1=-159.47 kJ·mol-1
NH2COONH4(s) ΔH1=-159.47 kJ·mol-1
反应II:NH2COONH4(s) ![]() CO(NH2)2(s)+H2O(g) ΔH2=+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH2=+72.49kJ·mol-1
请回答下列问题:
(l)写出CO2和NH3为原料生成尿素和气态水的热化学反应方程式_______,反应II自发进行的条件是_____。
(2)CO2和NH3为原料合成尿素的反应中影响CO2转化率的因素很多,下图为某待定条件下,不同水碳比[n(H2O)/n(CO2)]和温度影响CO2转化率变化的趋勢曲线。
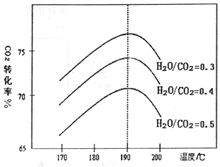
下列说法不正确的是__________。
A.温度升髙该反应平衡常数逐渐减小,移走部分尿素平衡向正方向移动
B.当温度低于190℃,随温度升髙CO2转化率逐渐增大,其原因可能是温度升高平衡向正方向移动
C.当温度髙于190℃后,随温度升髙CO2转化率逐渐减小,其原因可能是温度升高发生了副反应
D.其他条件相同时,为提髙CO2的转化率,生产中可以采取的措施是提高水碳比
(3)某研究小组为探究反应I中影响C(CO2)的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,t1时达到平衡,其c(CO2)随时间t变化趋势曲线如下图所示。则其逆反应的平衡常数为_____。若其他条件不变,t1时将容器体积压缩到1L,请画出t1t2时间段C(CO2)随时间t变化趋势曲线(t2时达到新的平衡)。__________
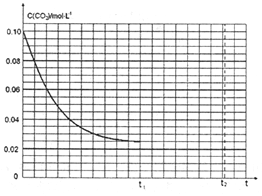
(4)电解尿素[CO(NH2)2]的碱性溶液制氢气的装置示意图如下图,请写出在A电极上发生的电极反应式_____。

查看答案和解析>>
科目: 来源: 题型:
【题目】氮气是一种很不活泼的气体,其根本原因是
A.氮元素的非金属性较弱 B.氮原子半径小,核对外层电子吸引力较强
C.氮气为双原子分子 D.使N≡N键断裂需要很高的能量
查看答案和解析>>
科目: 来源: 题型:
【题目】下列性质不属于甲烷性质的是( )
A. 完全燃烧时生成二氧化碳和水
B. 常温常压下能溶于水
C. 光照下能与卤素单质发生取代反应
D. 通常情况下,跟强酸、强碱和强氧化剂不反应
查看答案和解析>>
科目: 来源: 题型:
【题目】制备干燥的氨气所需的药品是( )
A. 饱和氨水、浓硫酸 B. NH4Cl稀溶液、NaOH稀溶液、碱石灰
C. NaOH溶液、NH4Cl晶体、浓H2SO4 D. NH4Cl固体、消石灰、碱石灰
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,在密闭容器里分别充入两种气体各1mol,在一定条件下充分反应后,恢复到原温度时,压强降低为开始时的1/4。则原混合气体可能是( )
A. H2和O2 B. HCl和NH3 C. H2和Cl2 D. CO和O2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中生成物的总能量高于反应物的总能量的是
A. Zn与稀硫酸反应放出氢气 B. 酸碱中和反应.
C. 硫在空气中燃烧 D. Ba(OH)2·8H2O与NH4Cl反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列反应中,水既不是氧化剂,也不是还原剂的是( )
A. 2Na+2H2O=2NaOH+H2↑ B. C12+H2O=HC1+HC1O
C. 2F2+2H2O=4HF+O2 D. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下所示:
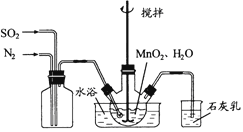
Ⅰ.制备MnSO4溶液:
在三颈烧瓶中加入4.35gMnSO4和足量的水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤、洗涤,得MnO2溶液。(N2不参与反应)
(1)制取MnSO4的化学方程式为_______________.
(2)反应过程中,为使SO2尽可能转化完全,在不改变固液投料的条件下,可采取的合理措施有________________.
(3)水浴加热的优点是____________。
Ⅱ.制备高纯MnCO3固体:
已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;pH=7.7时Mn(OH)2开始沉淀。
实验步骤: ①将所得MnSO4溶液与20.0mL 2.0mol/L的Na2CO3溶液混合,充分反应;②过滤,用少量水洗涤2~3次 ;③用少量C2H5OH洗涤;④低温 (低于100℃) 干燥,得固体3.45g。 (1) MnSO4溶液与Na2CO3溶液混合的正确操作为__________。(填字母代号)
a. 将Na2CO3溶液缓慢滴加到MnSO4溶液中,边加边搅拌
b. 将MnSO4溶液缓慢滴加到Na2CO3溶液中,边加边搅拌
c. 将Na2CO3溶液迅速倒入到MnSO4溶液中,并充分搅拌
d. 将MnSO4溶液迅速倒入到Na2CO3溶液中,并充分搅拌
(2)检验MnCO3固体是否洗涤干净的方法为______________。
(3) 用少量C2H5OH洗涤的目的是_______________。
(4) MnCO3的产率为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在100 ℃时,将0.40 mol二氧化氮气体充入一个2 L抽空的密闭容器中,发生反应:2NO2![]() N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用NO2表示的平均反应速率为__________mol·L1·s1。
(2)n3________(填“>”“<”或“=”)n4;该反应的平衡常数K的数值为___________(精确到0.1)。
(3)若在相同条件下最初向该容器中充入N2O4,要达到上述平衡状态,N2O4的起始浓度是______mol·L1。
(4)上述(3)达到平衡后N2O4的转化率为_______,混合气体的平均摩尔质量为____________。
(5)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2![]() N2O4的平衡常数将________(填“增大”“减小”或“不变”)。
N2O4的平衡常数将________(填“增大”“减小”或“不变”)。
(6)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将________(填“向左移动”、“向右移动”或“不移动”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com