
科目: 来源: 题型:
【题目】既可以用来鉴别甲烷和乙烯,又可以用来除去甲烷中混有的少量乙烯的操作方法( )
A.混合气通过盛酸性高锰酸钾溶液的洗气瓶
B.混合气通过盛足量溴水的洗气瓶
C.混合气通过盛蒸馏水的洗气瓶
D.混合气跟适量氯化氢混合
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组同学研究合成氨反应及氨水的性质如下:
(1)已知:N2(g)+3H2(g)=2NH3(g) △H =-92.4 kJ/mol
2H2(g)+O2(g)=2H2O(g) △H =-483.6kJ/mol
则氨气完全燃烧生成氮气和水蒸气的热化学方程式__________________________。
(2)如图是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是_______________(填“温度”或“压强”),判断L1、L2的大小关系:L1______L2(填“<”或“>”)。

(3)已知:在硫酸铜溶液中加入浓氨水,首先析出蓝色的碱式硫酸铜沉淀,氨水过量时此沉淀溶解,得到深蓝色的四氨合铜(Ⅱ)络离子,发生的离子反应如下:
a.2Cu2++ 2NH3·H2O+ SO42-=== 2NH4+ + Cu2(OH)2SO4↓
b.Cu2(OH)2SO4 + 8 NH3![]() 2[Cu(NH3)4]2++SO42-+2 OH-
2[Cu(NH3)4]2++SO42-+2 OH-
某小组设计如下实验:
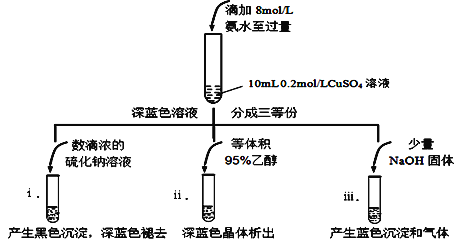
①试管ⅰ中反应的离子方程式_______________________________________。
②试管ⅱ中的深蓝色晶体是[Cu(NH3)4]SO4·H2O,该实验现象反映出该晶体的性质是______。
③请结合方程式解释试管ⅲ加入少量NaOH后产生蓝色沉淀和气体的原因_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一支25 mL的酸式滴定管中盛入0.1 mo1·L-1HCl溶液,其液面恰好在5 mL的刻度处。若把滴定管中的溶液全部放入锥形瓶中,然后以0.1 mo1·L-1NaOH溶液进行中和,则所需NaOH溶液的体积
A.等于20mLB.大于20mLC.小于20mLD.等于5mL
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,若使pH=3的盐酸与pH=9的Ba(0H)2溶液混合使其成为pH=7的溶液,混合时两溶液的体积比为( )。
A.1:60 B.3:1 C.100:l D.1:100
查看答案和解析>>
科目: 来源: 题型:
【题目】我国药学家屠呦呦因发现植物黄花蒿叶中含贫抗疟疾的物质——青蒿素而荣获2015年诺贝尔奖。科学家对青蒿素的结构进行进一步改良,合成药效更佳的双氢青蒿素、蒿甲醚。
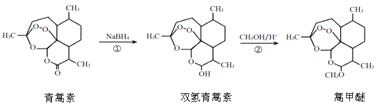
下列说法错误的是
A. 利用黄花蒿叶研究青蒿素结构的基本步骤为:分离、提纯→元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式
B. ①、②的反应类型分別为还原反应、取代反应
C. 双氢青蒿素在水中的溶解性大于青蒿素
D. 可用质谱法确定分子中含有何种官能团的信息
查看答案和解析>>
科目: 来源: 题型:
【题目】甲酸钙广泛用于食品、化工、石油等工业生产上,300~400℃左右分解.
Ⅰ、实验室制取的方法之一是:Ca(OH)2+2HCHO+H2O2=Ca(HCOO)2+2H2O+H2↑.
实验室制取时,将工业用氢氧化钙和甲醛依次加入到质量分数为30-70%的过氧化氢溶液中(投料物质的量之比依次为1:2:1.2),最终可得到质量分数98%以上且重金属含量极低的优质产品.
(1)过氧化氢比理论用量稍多,其目的是____________。
(2)反应温度最好控制在30-70℃之间,温度不宜过高,其主要原因是____________。
(3)制备时在混合溶液中要加入微量硼酸钠抑制甲醛发生副反应外,还要加入少量的Na2S溶液,加硫化钠的目的是____________。
(4)实验时需强力搅拌45min,其目的是____________;结束后需调节溶液的pH 7~8,其目的是____________,最后经结晶分离、干燥得产品.
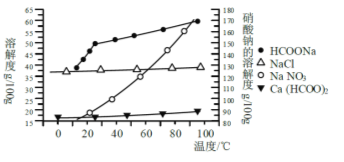
Ⅱ、某研究性学习小组用工业碳酸钙(主要成分为CaCO3;杂质为:Al2O3、FeCO3) 为原料,先制备无机钙盐,再与甲酸钠溶液混合制取甲酸钙.结合下图几种物质的溶解度曲线及表中相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0molL-1计算)。
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
请补充完整由碳酸钙制备甲酸钙的实验方案:
步骤一:称取13.6g甲酸钠溶于约20mL水,配成溶液待用,并称取研细的碳酸钙样品10g待用;
步骤二:____________;
步骤三:____________;
步骤四:过滤后,将滤液与甲酸钠溶液混合,调节溶液pH7-8,充分搅拌,所得溶液经过 、 、洗涤、60℃干燥得甲酸钙晶体。
提供的试剂有:a.甲酸钠,b.5molL-1硝酸,c.5molL-1盐酸,d.5molL-1硫酸,e.3%H2O2溶液,f.澄清石灰水。
查看答案和解析>>
科目: 来源: 题型:
【题目】有BaCl2和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl— 完全沉淀。反应中消耗xmolH2SO4、ymolAgNO3。据此得知原混合溶液中c(Na+)为
A. ![]() mol·L—1 B.
mol·L—1 B. ![]() mol·L—1
mol·L—1
C. ![]() mol·L—1 D.
mol·L—1 D. ![]() mol·L—1
mol·L—1
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)X、Y、Z三种液体的近似pH如图,下列判断正确的是___________。

A.X一定是酸或强酸弱碱盐溶液 B.Y一定是90℃时的纯水
C.Y液体一定呈中性 D.Z可能是Na2SiO3溶液
(2)物质的量浓度相同的三种溶液:①NH4Cl②氨水③NH4HSO4,c(NH4+)大小顺序正确的
是___________。
A.①>②>③ B.③>①>② C.②>③>① D.③>②>①
(3)用铂电极电解一定浓度的下列物质的水溶液,在电解后的溶液中加适量水,能使溶液浓度恢复到电解前浓度的是___________。
A.NaOH B.CuSO4C.K2S D.NaCl
(4)比较填空(选填“>"或“ <"或"=”)
①2H2(g)+O2(g)= 2H2O(g)△H1和2H2(g)+O2(g)= 2H2O(l)△H2的△H大小:△H1 __________△H2。
②等体积等PH的溶液:a.盐酸 b.硫酸,分別与足量NaOH溶液反应,消耗NaOH的物质的
量多少:a___________b。
③常温下两种溶液:a.pH=4盐酸 b.pH=4NH4Cl溶液,其中水的电离程度大小:a__________b。
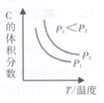
④已知某可逆反应aA(g)+bB(g)![]() cC(g)+dD(g)。当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图所示,则反应物和生成物的化学计量数之和:a+b ______c+d。
cC(g)+dD(g)。当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图所示,则反应物和生成物的化学计量数之和:a+b ______c+d。
(5)在一定体积的密闭容器中加入1molCO2和1mol H2,进行如下化学反应:CO2(g)+ H2(g) ![]() CO(g)+H2O(g) ,其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g) ,其化学平衡常数K和温度T的关系如下表:
T(℃) | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K=__________________________。
②反应为___________反应(填“吸热”或“放热”)。
③某温度下,平衡时各物质的浓度有如下关系:3[c(CO2)c(H2)] =5[c(CO)(H2O)],判断此时的反应温度为___________℃。
④800℃,向容器内充入lmolCO2、lmolH2、lmol CO、lmolH2O,此刻反应的v正___________ v逆(填“>"或“<”或“=”)
(6)下图所示为用惰性电极电解100mL 0.5mol·CuSO4溶液的装置,b电极上的电极反应式为______。若a电极共产生56mL(标准状况)气体,则所得溶液的pH =___________(不考虑溶液体积变化)。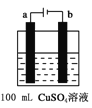
查看答案和解析>>
科目: 来源: 题型:
【题目】以下物质间的转化通过一步反应不能实现的是( )
A.HCl →Cl2→HClO→NaClO
B.Na→Na2O2→Na2CO3→NaHCO3
C.Si→SiO2→H2SiO3→Na2SiO3
D.Al→NaAlO2 →Al(OH)3→Al2O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com