
科目: 来源: 题型:
【题目】下列实验的反应原理用离子方程式表示正确的是( )
A. 室温下,测得氯化铵溶液pH<7,证明一水合氨是弱碱:NH![]() +2H2O===NH3·H2O+H3O+
+2H2O===NH3·H2O+H3O+
B. 用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O===2AlO![]() +3H2↑
+3H2↑
C. 用碳酸氢钠溶液检验水杨酸中的羧基:
 +2HCO
+2HCO![]() →
→ +2H2O+2CO2↑
+2H2O+2CO2↑
D. 用高锰酸钾标准溶液滴定草酸:2MnO![]() +16H++5C2O
+16H++5C2O![]() ===2Mn2++10CO2↑+8H2O
===2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
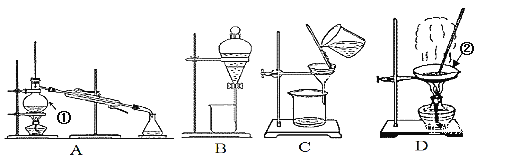
(1)装置A中仪器①的名称是______,装置D中仪器②的名称是______。
(2)从氯化钾溶液中得到氯化钾固体,应选择装置_____(填代表装置图的字母,下同)。
(3)分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)(已知四氯化碳和甲苯互溶),应选择装置______。
(4)从碘水中分离出I2,选择装置______,该装置的主要仪器名称是______,若用CCl4作为萃取剂,充分振荡后静置,观察到的现象是:______________________。
(5)装置C和D中均用到了玻璃棒,它们的作用各是什么?________。
查看答案和解析>>
科目: 来源: 题型:
【题目】温度为T1时,在三个容积均为1 L的恒容密闭容器中仅发生反应:2NO2(g) ![]() 2NO(g)+O2(g)(正反应吸热)。实验测得:v正= v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是
2NO(g)+O2(g)(正反应吸热)。实验测得:v正= v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是

A.达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为4∶5
B.达平衡时,容器Ⅱ中![]() 比容器Ⅰ中的大
比容器Ⅰ中的大
C.达平衡时,容器Ⅲ中NO的体积分数小于50%
D.当温度改变为T2时,若k正=k逆,则 T2<T1
查看答案和解析>>
科目: 来源: 题型:
【题目】高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室里欲用KMnO4固体来配制240mL 0.1 molL-1的KMnO4酸性溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、_________
②配制过程中玻璃棒所起的作用是_________
③下列操作对实验结果的影响偏小的是______(填序号)
a.加水定容时俯视刻度线 b.容量瓶内壁附有水珠而未干燥处理
c.若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶
d. 颠倒摇匀后发现凹液面低于刻度线又加水补上
④下列为打乱了的操作示意图,请按先后顺序正确排序_______。
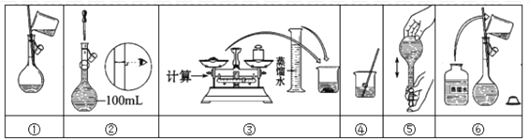
(2)用上述酸性KMnO4溶液来测定FeSO4溶液中Fe2+的物质的量浓度。
①配平该反应的化学方程式:
__FeSO4+ KMnO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O
②该反应中的氧化剂是__________,氧化产物是__________
③若消耗3.16gKMnO4,则该反应转移的电子数目为______
(3)已知反应:①Cl2+2KBr=2KCl+Br2,②2KMnO4+16HCl(浓) =2KCl + 2MnCl2+ 5Cl2↑+8H2O,③Br2+K2S=2KBr+S。
①下列说法正确的是___。
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为KMnO4>Cl2>Br2>S
C.反应②中还原剂与氧化剂的物质的量之比为8:1
D.反应③中1mol还原剂被氧化则转移电子的物质的量为2mol
②用单线桥法标出反应②中电子转移的方向和数目_____。
2KMnO4+16HCl(浓) = 2KCl + 2MnCl2+ 5Cl2↑+8H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】向盛有50 mL 1.00 mol·L1 盐酸的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如图所示,下列说法不正确的是
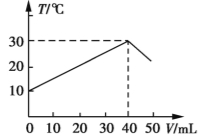
A.该实验表明化学能可以转化为热能
B.NaOH溶液的浓度大于1.00 mol·L1
C.V=50 mL时,混合溶液的pH>7
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室通常用MnO2和浓盐酸共热制取Cl2,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)该反应的氧化剂是_____________,氧化产物是_____________,用双线桥或单线桥法表示上述反应电子转移的方向和数目____________________________________。
(2)计算当有73.0克HCl被氧化时,消耗MnO2的质量为_____________。
(3)在反应MnO2+4HCI![]() MnCl2+C12↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是____________。
MnCl2+C12↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2 ,则下列说法中正确的是( )
2KClO3 + H2C2O4 + H2SO4 ![]() 2ClO2↑ + K2SO4 + 2CO2↑ + 2H2O
2ClO2↑ + K2SO4 + 2CO2↑ + 2H2O
A. KClO3在反应中是还原剂
B. 1molKClO3参加反应,在标准状况下能得到22.4L气体
C. 在反应中H2C2O4 既不是氧化剂也不是还原剂
D. 1molKClO3参加反应有1mol电子转移
查看答案和解析>>
科目: 来源: 题型:
【题目】氰(CN)2的结构简式为N≡C—C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间。下列有关反应的化学方程式不正确的是( )
A. (CN)2+H2=2HCN
B. MnO2+4HCN=Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合液中通入少量Cl2:Cl2+2KCN=2KCl+(CN)2
查看答案和解析>>
科目: 来源: 题型:
【题目】R元素的原子有三个电子层,M层电子数是K层电子数的3倍,对R元素的判断不正确的是 ( )
A. R元素处于第三周期ⅥA族 B. R元素是非金属元素
C. 原子核外共有14个电子 D. R元素最低化合价为-2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com