
科目: 来源: 题型:
【题目】下列变化过程,属于放热反应的是( )
① 液态水变成水蒸气 ② 酸碱中和反应 ③ 浓H2SO4稀释 ④ 固体NaOH溶于水 ⑤ H2在Cl2中燃烧 ⑥ 弱酸电离
A. ②③④⑤ B. ②③④ C. ②⑤ D. ①③⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)![]() 2Z(g) ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是( )
2Z(g) ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是( )
A. 升高温度,X的体积分数减小
B. 增大压强(缩小容器体积),Z的浓度不变
C. 保持容器体积不变,充入一定量的惰性气体,Y的浓度不变
D. 保持容器体积不变,充入一定量的Z,X的体积分数增大
查看答案和解析>>
科目: 来源: 题型:
【题目】赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热有如下反应:Cu2S+2Cu2O![]() 6Cu+SO2↑。下列关于该反应的说法中,正确的是
6Cu+SO2↑。下列关于该反应的说法中,正确的是
A. 每生成22.4L SO2,反应中转移6 mol电子
B. Cu2S在反应中既是氧化剂,又是还原剂
C. Cu既是氧化产物又是还原产物
D. 每生成19.2 g Cu,反应中转移0.6 mol电子
查看答案和解析>>
科目: 来源: 题型:
【题目】250℃时,14gCO2和H2O(g)的混合气体与足量的Na2O2反应,反应后固体质量增加了6g,则原混合物的平均相对分子质量为
A. 36 B. 22 C. 28 D. 42
查看答案和解析>>
科目: 来源: 题型:
【题目】在反应:K2Cr2O7+14HCl(浓)===2KCl+2CrCl3+3Cl2↑+7H2O中,用氧化还原反应的知识分析:____是氧化剂,_____是还原剂,____是还原产物,____是氧化产物,电子转移总数是___e-,用“双线桥法”表示反应中电子转移的方向和数目:__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】300℃时,将100mL由H2O、CO2和N2组成的混合气体通入盛有足量Na2O2的密闭容器中(容器体积保持不变),充分反应后恢复到原温度时容器内的压强变为原来的4/5,则原混合气体中N2的体积分数为
A. 33.3% B. 40% C. 60% D. 75%
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA
B. 标准状况下,18 g H2O所占的体积约是22.4 L
C. 32 g O2在标准状况下所占的体积约为22.4 L
D. 2.4g金属镁变为镁离子时失去的电子数为0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 海洋约占地球表面积的71%,所以地球上不缺水,人类可以随意使用水资源,不必节约
B. 海水淡化的主要方法有蒸馏法、电渗析法和离子交换法
C. 海水淡化的各种方法中,蒸馏法的成本比较低
D. 以上说法都正确
查看答案和解析>>
科目: 来源: 题型:
【题目】分析下表中三种气体物质的有关数据,下列说法不正确的是
物质 | 质量 | 体积 | ||
0℃,101kPa | 20℃,101kPa | 0℃,202kPa | ||
H2 | 2 | 22.4 | 24.0 | 11.2 |
O2 | 32 | 22.4 | 24.0 | 11.2 |
CO2 | 44 | 22.3 | 23.9 | 11.2 |
A. 物质的量相同的三种气体,在相同的条件下,其体积约相等
B. 相同的条件下,体积相同的三种气体,其质量不同
C. 相同的条件下,体积相同的三种气体,因其质量不同,故气体分子数目也不同
D. 质量相同的三种气体,在相同的条件下,其体积一定不同
查看答案和解析>>
科目: 来源: 题型:
【题目】在80 ℃时,将0.40 mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4![]() 2NO2 ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
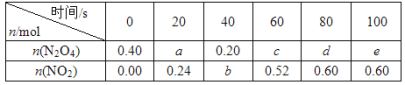
(1)计算20~40 s内用N2O4表示的平均反应速率为_________mol/( L s)。
(2)计算在80℃时该反应的平衡常数K=__________(请注明单位)。
(3)反应进行至100 s后将反应混合物的温度降低,混合气体的颜色______(填“变浅”“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有_________(填序号)。
A.增大N2O4的起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。
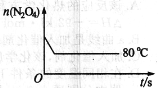
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com