
科目: 来源: 题型:
【题目】浓度为0.1 mol·L-1的HCl溶液VmL,加水稀释到2VmL,取出10 mL,这10 mL溶液中含有c(H+)( )
A. 0.5 mol·L-1 B. 0.01 mol·L-1 C. 0.02 mol·L-1 D. 0.05 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质性质与应用对应关系正确的是
A. KAl(SO4)2 12H2O能水解生成Al(OH)3胶体,可用作净水剂
B. SO2有漂白、杀菌性能,可在食品加工中大量使用
C. MnO2有较强的氧化性,可作H2O2分解的氧化剂
D. Si是半导体材料,可用于制光导纤维
查看答案和解析>>
科目: 来源: 题型:
【题目】已知单质硫在通常条件下以S8(斜方硫)的形式存在,其结构如图所示。
S8:![]() (冠状)
(冠状)
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)。能量和反应过程的关系可用下图简单表示(图中的ΔH表示生成1 mol产物的数据)。
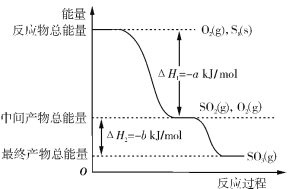
试根据上图回答下列问题:
(1)写出表示S8(s)的燃烧热的热化学方程式____________。
(2)写出SO3分解生成SO2和O2的热化学方程式____________。
(3)若已知S—O的键能为d kJ/mol,O![]() O的键能为e kJ/mol,则S8分子中S—S键的键能为__________。
O的键能为e kJ/mol,则S8分子中S—S键的键能为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y![]() 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
A. 33% B. 40% C. 50% D. 65%
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于化学与生产、生活的认识错误的是
A. CO2、SO2、N2等均是造成温室效应的气体
B. 节能减排符合低碳经济的要求
C. 使用清洁能源是防止酸雨发生的重要措施之一
D. 大量焚烧田间秸秆会污染空气
查看答案和解析>>
科目: 来源: 题型:
【题目】电解硫酸钠溶液生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1∶2,以下说法正确的是( )

A. a极与电源的负极相连
B. a电极反应式:2H2O+2e-= H2↑+2OH-
C. 离子交换膜d为阴离子交换膜
D. 产物丙为硫酸溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3。Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用。某科研小组用该原理处理污水,设计的装置如图所示。下列说法正确的是
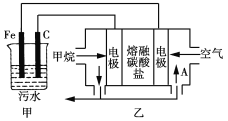
A.为了增加污水的导电能力,应向污水中加入适量的CH3CH2OH溶液
B.甲装置中Fe电极的反应为Fe-3e-=Fe3+
C.为了使燃料电池乙长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环的物质A为CO2
D.当乙装置中有1.6 g CH4参加反应时,C电极理论上生成气体的体积在标准状况下为4.48 L
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列四种化学操作从左到右名称比较合理分别是_________ (填序号)。
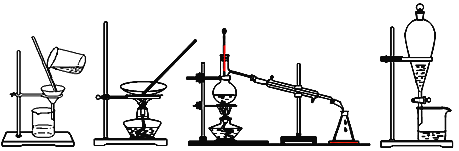
A.过滤、结晶、蒸馏、分液
B.过滤、蒸馏、结晶、分液
C.结晶、蒸馏、过滤、分液
D.分液、蒸馏、结晶、过滤
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上:
A.过滤 B.结晶 C.分液 D.蒸馏 E.萃取分液
① ____________分离水和四氯化碳的混合物
② ___________ 分离饱和氯化钾溶液和沙子的混合物
③ ___________ 从硝酸钾和氯化钠的混合溶液中获得硝酸钾
④ ___________ 分离酒精(沸点为为78.10C)和甲苯(沸点为110.60C)的混合物
⑤ ___________ 用四氯化碳提取溴水中的溴单质
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需配制0.5 mol·L-1的烧碱溶液500mL,根据配制的过程,完成填空:
(1)根据计算得知,所需NaOH固体用托盘天平称出的质量为___________g。
(2)配制溶液的过程中,有以下操作。其中正确的是___________ (填序号)。
A.将氢氧化钠固体放在纸片上称量
B.在烧杯中溶解氢氧化钠固体后,立即将溶液倒入容量瓶中
C.将溶解氢氧化钠的烧杯用蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中
D.定容时发现所配溶液超过刻度线,用胶头滴管吸取溶液使液面与刻度线相平
(3)玻璃棒在该实验中的作用有:
①_______________。
②_______________。
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?
①若没有将洗涤液转移到容量瓶的操作_______________;
②若加蒸馏水时不慎超过了容量瓶的刻度_______________;
③若定容时俯视刻度线_______。
④容量瓶中使用前有少量蒸馏水没有干燥_______。
(5)取所配溶液24.0 mL可以中和_______mL的12mol/L浓盐酸。标准状况下_______L的HCl气体溶于水可配成这种浓度的浓盐酸100 mL。
(6)计算填空:已知MnO2+4HCl (浓)![]() MnCl2+Cl2↑+2H2O。若用二氧化锰消耗此12mol/L 的浓盐酸100 mL制备氯气,理论上需要二氧化锰_______g,可以制得氯气在标准状况下的体积为_______L。该反应是否是氧化还原反应,请判断并说出理由_______。
MnCl2+Cl2↑+2H2O。若用二氧化锰消耗此12mol/L 的浓盐酸100 mL制备氯气,理论上需要二氧化锰_______g,可以制得氯气在标准状况下的体积为_______L。该反应是否是氧化还原反应,请判断并说出理由_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用控制n(H2S):n(FeCl3)=1:2反应得到的产物再用电解法制氢,其工作原理如图所示。下列有关的说法错误的是( )
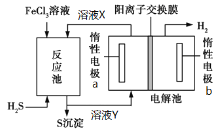
A. 惰性电极a发生氧化反应
B. Fe(OH)3胶体中滴加溶液X,先有沉淀后沉淀溶解
C. 溶液Y加热蒸发灼烧最终得到Fe2O3
D. 电解池总反应的离子方程式为2Fe2++2H+![]() 2Fe3++H2↑
2Fe3++H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com