
科目: 来源: 题型:
【题目】在容积固定的容器中发生反应:CO(g)+2H2(g)![]() CH3OH(g) ΔH<0,各物质的浓度如表所示:
CH3OH(g) ΔH<0,各物质的浓度如表所示:
浓度 时间 | c(CO)/ mol·L-1 | c(H2)/ mol·L-1 | c(CH3OH)/ mol·L-1 |
0 | 0.8 | 1.6 | 0 |
2 min | 0.6 | x | 0.2 |
4 min | 0.3 | 0.6 | 0.5 |
6 min | 0.3 | 0.6 | 0.5 |
下列说法不正确的是( )
A. 2~4 min内用H2表示的平均反应速率为0.3 mol·L-1·min-1
B. 达到平衡时,CO的转化率为62.5%
C. 反应在第2 min时改变了条件,可能是加入了催化剂
D. 反应在第2 min时改变了条件,可能是增加了H2的浓度
查看答案和解析>>
科目: 来源: 题型:
【题目】某磷肥厂利用某磷矿石[Ca3(PO4)2]制取磷肥[Ca(H2PO4)2]并综合利用副产物生产水泥的工艺流程如图:

(1)将磷矿石制成磷肥的目的是 ______ ,有关的化学方程式为 ______ .
(2)在该工艺流程中高硫煤粉不需要脱硫,理由是 ______ .
(3)水泥属于 ______ 材料.(填“A”或者“B”:A.新型无机非金属材料B.传统无机非金属材料)
(4)工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为放热反应.现将2molSO2、1molO2充入体积为2L的密闭容器中充分反应,放出热量98.3kJ,此时测得SO2的物质的量为1mol.则该热化学方程式为 _______________________ ,平衡常数K为 ______.
(5)工业上用接触法制硫酸,最后的产品是98%的硫酸或组成为2H2SO4SO3的发烟硫酸(H2SO4和H2SO4SO3的混合物,其中SO3的质量分数约为29%).若98%的浓硫酸可表示为SO3aH2O,含SO329%的发烟硫酸可表示为bSO3H2O,则a= ______ ,b= ______.
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是元素周期表的一部分,表中所列字母分别代表一种元素

回答下列问题:
(1)h元素的名称是_________,九种元素中金属性最强的是_________(填元素符号)。
(2)f的最高价氧化物对应的水化物的化学式___________(填化学式)。
(3)b、c、d、e的原子半径依次___________(填增大或减小)。
(4)e、h元素的氢化物中,热稳定性大的是_________(填氢化物的化学式)。
(5)工业上冶炼g元素的单质的化学方程式_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组的同学发现《高中化学(必修1)》中学习的单质及其化合物(或其溶液)存在如图的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;F为淡黄色粉末,化合物H和I通常状况下呈气体;反应①是化工生产中的一种重要固氮反应.
请用化学用语回答下列问题: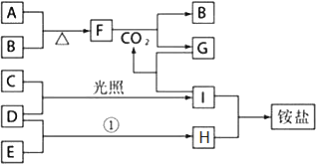
(1)B是 ______ ,化合物G的焰色反应为 ______ ;
(2)将F溶于水后形成的溶液可吸收C,写出该反应的离子方程式 ______________________________ ;
(3)写出实验室制取氨气的化学方程式: ______________________________ ,收集氨气应使用 ______ 法,要得到干燥的氨气通常选用 ______ 做干燥剂.
查看答案和解析>>
科目: 来源: 题型:
【题目】Mg(ClO3)2加入到含有KSCN的FeSO4酸性溶液中立即出现血红色,写出相关反应的离子方程式: _______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质的说法中正确的是
A.工业上利用氨气制硝酸属于人工固氮
B.锌锰干电池、燃料电池、铅蓄电池都属于二次电池
C.在食品包装袋内放入铁粉保鲜剂可以防止食品因氧化而变质
D.碳酸铵俗称碳铵,是常见的铵盐之一,应避免与碱性肥料混合施用
查看答案和解析>>
科目: 来源: 题型:
【题目】碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,这时候,观察到的现象是___________________________;
(2)某学生在一次分液操作中发现上下层溶液都是无色液体,无法知道分液漏斗中的液体哪一层是有机层,哪一层是水层,请你用简单的方法帮他鉴别出来,写出有关步骤及判断____________________________;
(3)在容量瓶的使用方法中,下列操作正确的是____________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(4)上面实验中用到一定物质的量浓度的稀硫酸,若配制0.5mol/L的硫酸溶液450mL,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为_______ mL,如果实验室有15mL、20mL、50mL量筒,应选用________ mL量筒最好。
(5)下面操作造成所配稀硫酸溶液浓度偏高的是_____________
A.溶解的时候溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于铝的性质和用途描述不正确的是
A.铝有很好的延展性且是良导体,所以常用作导线
B.用酒精灯外焰加热铝箔,可以看到少量液滴悬而不落,说明铝的熔点较高
C.铝合金质轻,强度大,耐腐蚀,可以用作门窗
D.铝有较强的抗腐蚀性,是因为铝的表面能形成致密的氧化膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com