
科目: 来源: 题型:
【题目】在光照的条件下,将等物质的量的甲烷和氯气混合充分反应后,得到产物的物质的量最多的是( )
A. CH2Cl2 B. CHCl3 C. CCl4 D. HCl
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是金属钨的晶胞结构模型图。实验测得金属钨的密度为19.3g.cm-3,钨的相对原子质量为183.9.假定金属钨为等径的刚性球。(必须列式计算)
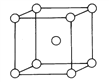
(1)每个晶体分摊到的钨原子个数;
(2)计算晶胞的边长a和钨的原子半径r;
(3)计算金属钨晶胞的空间利用率。
查看答案和解析>>
科目: 来源: 题型:
【题目】电子表所用纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应如下:锌极:Zn+2OH--2e-=Zn(OH) 2,氧化银极:Ag2O+H2O+2e-=2Ag+2OH-,下列说法正确的是
A.锌为正极,被氧化
B.Ag2O是正极,发生还原反应
C.电流从Zn极经导线流向Ag2O极
D.Zn为负极,被还原
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A. 含有离子键的化合物必是离子化合物
B. 具有共价键的化合物就是共价化合物
C. 离子化合物中可能含有共价键
D. 由金属和非金属元素组成的化合物一定是离子化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】以下各组溶液中Cl-的物质的量浓度与300 mL 1 mol/L NaCl溶液中Cl-的物质的量浓度相同的是
A. 100 mL 1 mol/L AlCl3溶液 B. 200 mL 1 mol/L MgCl2溶液
C. 100 mL 0.5 mol/L CaCl2溶液 D. 100 mL 2 mol/L KCl溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】填写下列空格:
(1)标准状况下,5.6g N2的体积为______L,含有的氮原子数为______.
(2)同温、同压下,质量相等的SO2和CO2相比较,体积之比为____,已知SO2和CO2均为酸性氧化物,写出SO2与足量NaOH溶液反应的化学方程式______________________________.
(3)由硫酸钾、硫酸铝和硫酸组成的混合溶液,其c(H+)=0.1molL﹣1,c(Al3+)=0.4molL﹣1,c(SO42﹣)=0.9molL﹣1,则c(K+)为_____molL﹣1
(4)在100mLAl2(SO4)3溶液中含0.6molSO42﹣,Al3+的物质的量浓度为______mol/L,从中取出25mL加水稀释到100mL,则稀释后的溶液中SO42﹣的物质的量浓度为______.
(5)19 g某二价金属的氯化物ACl2中含有0.4mol Cl-,则ACl2的摩尔质量_________,画出A2+的结构示意图____________。
(6)在一定温度和压强下,5体积气体A2跟15体积的气体B2完全化合生成10体积某气体C,则该气体C的化学式为(用A、B表示)__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某原电池装置如图所示。下列有关叙述中,正确的是 ( )
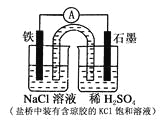
A. Fe作正极,发生氧化反应
B. 负极反应:2H++2e-===H2↑
C. 工作一段时间后,两烧杯中溶液pH均不变
D. 工作一段时间后,NaCl溶液中c(Cl-)增大
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,将固体X和气体Y各0.16 mol充入2L密闭容器中,发生反应:X(s)+Y(g)![]() 2 Z(g),一段时间后达到平衡。反应过程中测定的数据如下表:
2 Z(g),一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )。
A. 反应0~2 min内Z的平均速率v(Z) =0.04 molL﹣1min﹣1
B. 容器内压强保持不变时反应达到平衡
C. 该温度下,增加X的量,正反应速率加快
D. 降低Z 的浓度,一段时间后,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列氧化还原反应相关问题:
I.配平下面的氧化还原方程式:_______
___ Na2SO3+____ KIO3+____ H2SO4 =____ Na2SO4+____ K2SO4+____ I2+____ H2O
II.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为
![]() (浓)
(浓)![]()
![]() 。
。
(1)请分析该反应中电子转移的情况(用双线桥表示)_______________。
(2)浓盐酸在反应中显示出来的性质是________(填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
若标准状况下产生4.48L Cl2,则参加反应的KClO3的质量为_______g,被氧化的盐酸的物质的量为________mol,转移电子的物质的量为________mol。
(3)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是Cl2的________倍。(提示:ClO2与Cl2消毒时氯元素都被还原为最低价)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com