
科目: 来源: 题型:
【题目】1 000 mL某待测溶液中除含有0.2 mol·L-1的Na+外,还可能含有下列离子中的一种或多种:
阳离子 | K+、NH |
阴离子 | Cl-、Br-、CO |
现进行如下实验操作(每次实验所加试剂均过量):
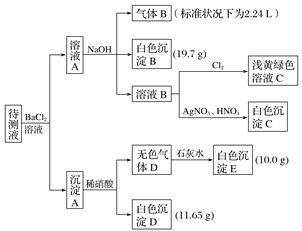
(1)写出生成白色沉淀B的离子方程式:__________________________________。
(2)待测液中肯定不存在的阳离子是________________。
(3)若无色气体D是单一气体:判断原溶液中K+是否存在____(填“是”或“否”),若存在,求其物质的量浓度的最小值,若不存在,请说明理由:________________________。
(4)若无色气体D是混合气体:
①待测液中一定含有的阴离子是________________。
②沉淀A中能与稀硝酸反应的成分是____________(写化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚铜是重要的铜盐系列化工产品,广泛应用于石油化工、有机合成等行业。CuCl晶体呈白色,微溶于水,不溶于稀盐酸和乙醇,露置于潮湿空气中易水解氧化为绿色的[Cu 2(OH)3C1],见光易分解。某研究小组以CuCl2(含少量Fe2+)粗品为原料制取CuCl,设计的合成路线如下:
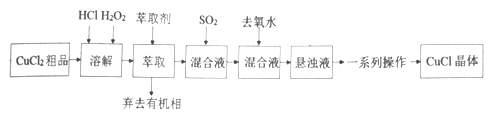
己知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮。
②CuCl在溶液中存在:CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)。
[CuCl3]2-(aq)。
请回答:
(1)下列叙述正确的是__________。
A.CuCl2原料中含有的Fe2+等杂质经氧化、萃取几乎都在有机相中被除去
B.加入萃取剂后,混合物转移至分液漏斗中,塞上玻璃塞,如图用力振摇![]()
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.用浓盐酸洗涤分液后的有机相时,需在分液漏斗中进行
(2)上述合成路线中,SO2通入混合液的实验装置如下图所示:
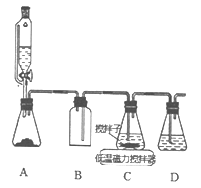
①装置D的作用是_______________。
②C中反应的离子方程式为_____________。
(3)上述合成路线中,向混合液中加入大量去氧水的目的是________________。
(4)上述合成路线中,一系列操作包括:抽滤、洗涤、干燥。干燥时应注意密封、____________。
(5)现称取l.200g产品,用硫酸酸化的硫酸铁溶解,并稀释成250mL。每次用移液管移取25.00mL溶液于锥形瓶中,用0.01000,mol·L-1KmnO4溶液滴定平均消耗24.00mL。
①用移液管吸取25.00mL溶液后,把溶液转移到锥形瓶中的具体操作为____________。
②产品中CuCl的纯度为__________(本实验条件下,Cl-难于被MnO4-氧化)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
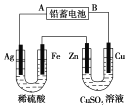
(1)A是铅蓄电池的___________极,铅蓄电池正极反应式为___________,放电过程中电解液的密度___________ (填“减小”、“增大”或“不变”)。
(2)Ag电极的电极反应式是___________,该电极的电极产物共____________g。
(3)Cu电极的电极反应式是____________,CuSO4溶液的浓度____________(填“减小”、“增大”或“不变”)
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示___________。

a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
查看答案和解析>>
科目: 来源: 题型:
【题目】肼(N2H4)可作为火箭发动机的燃料。
(1)肼(N2H4)与氧化剂N2O4(l)反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)===N2O4(l) ΔH1=195 kJ·mol1
②N2H4(l)+O2(g)===N2(g)+2H2O(g) ΔH2=534 kJ·mol1
试计算1 mol肼(l)与N2O4(l)完全反应生成N2和水蒸气时放出的热量为________,写出肼(l)和N2O4(l)反应的热化学方程式:________________________________。
(2)有关肼化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ):
N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需的能量是________ kJ。

查看答案和解析>>
科目: 来源: 题型:
【题目】将20mL 0.5mol·L-1盐酸与一块状大理石反应,下列的措施不能提高化学反应速率的是( )
A. 加入10mL 3mol·L-1盐酸
B. 给反应混合物加热
C. 将所用的大理石研磨成粉末
D. 加入10mL蒸馏水
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A. 利用高纯度硅制造的太阳能电池板可将光能直接转化为电能
B. 胶体的本质特征是丁达尔效应
C. 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质
D. 宋·王希孟《千里江山图》卷中的绿色颜料铜绿的主要成分是氢氧化铜
查看答案和解析>>
科目: 来源: 题型:
【题目】NO能否与Na2O2反应?如果能反应,产物是什么?某兴趣小组对此进行探究。
【查阅资料】①NO不与碱反应;②亚硝酸盐除浅黄色的AgNO2难溶于水外,其余易溶于水;③2NaNO3![]() 2NaNO2+O2↑,NaNO2热稳定性很高。
2NaNO2+O2↑,NaNO2热稳定性很高。
【实验探究Ⅰ】兴趣小组的同学经讨论设计了如下图所示实验:
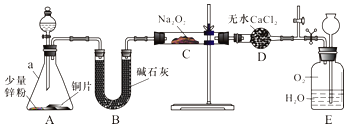
(1)仪器a的名称是 ;干燥管D的作用是 。
(2)从分液漏斗中加稀硝酸之前,先加入少量稀硫酸让A中锌粉完全溶解,其目的是 。
(3)若无B装置,后果是 。
(4)实验观察到C中固体颜色变白,E中气体先变红棕色,最终又变无色。E中总反应的化学方程式是 。
【实验探究Ⅱ】 该兴趣小组进一步探究C中生成的白色固体的成分。
(5)提出假设:假设1. 白色固体只有NaNO2;假设2. 白色固体只有 ;
假设3. 白色固体是两种物质的混合物。
(6)实验验证:①要证明假设2是否成立,实验操作、现象和结论是____________________。
②为证明是假设1还是假设3成立,称取C中生成的白色固体ag置于坩埚中(坩埚质量为cg),用酒精灯加热至质量不再改变,冷却后称得坩埚和剩余固体总质量为bg,假设3成立时b-c的数字范围是 。(用含a的不等式表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】现含有NaCl、MgCl2、CaCl2的混合液,某同学欲提取纯净的NaCl晶体,设计了如下实验:
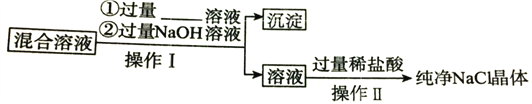
请回答下列问题:
(1)写出沉淀中所含物质的化学式_________,①中加入的过量试剂为_____。
(2)上述流程中,加入过量稀盐酸的目的是______________。
(3)操作I的名称是_____,操作Ⅱ的名称是_____。
(4)操作I的要点是一帖二低三靠,其中二低是指__________,____________。操作Ⅱ中当______(填仪器名称)中____________________________(填现象)时停止加热。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列现象或事实不能用同一原理解释的是( )
A.浓硝酸和氯水用棕色试剂瓶保存
B.硫化钠和亚硫酸钠固体长期暴露在空气中变质
C.Cl2和SO2都能使品红溶液褪色
D.SO2和Na2SO3溶液都能使溴水褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com