
科目: 来源: 题型:
【题目】一定条件下,将SO2和O2充入体积为2L的密闭容器中,发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:
2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:

回答下列问题:
(1)用 SO2表示0~15min的平均反应速率为__________。降低温度,SO2的转化率_________,化学反应速度_____________。(填“增大”“减小”或“不变”)。
(2)反应处于平衡状态的时间是 ________。则该反应正反应为_________(填“吸热”或“放热”)反应。
(3)反应进行至20min时,曲线发生变化的原因是 _____________(用文字表达);10~15min的曲线变化的原因可能是_____(填写编号)。
a.加了催化剂 b.升高温度 c.降低温度 d.增加SO3的物质的量
(4)在相同的温度时,在该2L的密闭容器中充入的是0.1mol的SO3,0.05mol的O2,0.05的SO2,平衡时若想SO2的体积分数与上述平衡时相同,则应再加入(填SO2、O2、SO3 ) __________,为_________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4 L水含有的水分子数为NA
B. 常温常压下,22 g CO2含有的CO2分子数为0.5NA
C. 标准状况下,32 g O2和CO2的混合气体含有的氧原子数为2NA
D. 40 g NaOH溶解在1 L水中,得到溶液的物质的量浓度为1 mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】为确定Fe和Cu混合物样品的组成,称取四份该样品分别加入相同浓度FeCl3 溶液200mL,充分反应,剩余沉淀的质量如下表:
实验序号 | I | II | Ⅲ | IV |
FeCl3溶液体积(mL) | 200 | 200 | 200 | 200 |
样品质量(g) | 9.36 | 12.48 | 15.6 | 18.72 |
沉淀质量(g) | 6.40 | 9.60 | 12.8 | 15.92 |
(1)样品中物质的量之比n(Fe)∶n(Cu) =_________。
(2)FeCl3溶液的物质的量浓度c(FeCl3)=_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列各反应中,盐酸既表现出酸性又表现出氧化性的是
A. HCI+NaOH===NaCl+H2O B. Zn+2HCl===ZnCl2+H2↑
C. HCl+AgNO3==AgCl↓+HNO3 D. MnO2+4HCl(浓) ![]() MnCl2+C12↑+2H2O
MnCl2+C12↑+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】大多数有机物分子里的碳原子与碳原子或碳原子与其他原子相结合的化学键是( )
A. 只有非极性键 B. 只有极性键
C. 非极性键和极性键 D. 只有离子键
查看答案和解析>>
科目: 来源: 题型:
【题目】将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为________。
(2)该溶液中NaOH的质量分数为________。
(3)从该溶液中取出10 mL,溶液的密度为________,含NaOH的物质的量为________。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________。
(5)标准状况下,1.7 g NH3标准状况下________ L H2S含有相同数目的氢原子。
(6)某气体氧化物的化学式为RO2,标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为________,R的相对原子质量为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是______________________。
在此过程中,两个电极上质量的变化值:阴极________阳极(填“>”“<”或“=”)。
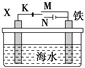
(3)利用如图所示的装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于________(填“M”或“N”)处。若X为锌,开关K置于M处,该电化学防护法称为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g)![]()
![]() N2(g)+CO2(g)△H=-373.2KJ/mol,达到平衡后,为提高NO的转化率和该反应的速率,可采取的措施是
N2(g)+CO2(g)△H=-373.2KJ/mol,达到平衡后,为提高NO的转化率和该反应的速率,可采取的措施是
A. 加催化剂同时升高温度
B. 加催化剂同时增大压强
C. 升高温度同时充入N2
D. 降低温度同时增大压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com