
科目: 来源: 题型:
【题目】下列物质分类正确的是
A. SO2、SiO2、CO均为酸性氧化物 B. 稀豆浆、硅酸、氯化铁溶液均为胶体
C. 烧碱、冰醋酸、蔗糖均为电解质 D. 盐水、水玻璃、氨水均为混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】在银锌原电池中,以硫酸铜为电解质溶液,锌为极,电极上发生的是反应(“氧化”或“还原”).电极反应式为 , 锌片上观察到的现象为银为极,电极上发生的是反应(“氧化”或“还原”),电极反应式是 , 银片上观察到的现象是 . 
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应4NH3+5O2![]() 4NO+6H2O(g),下列叙述正确的是
4NO+6H2O(g),下列叙述正确的是
A.若单位时间生成x mol NO的同时,消耗1.5x mol H2O,则反应达到平衡状态
B.达到平衡状态后,NH3、O2、NO、H2O(g)的物质的量之比为4∶5∶4∶6
C.达到平衡状态时,若增加容器体积,则反应速率增大
D.达到平衡时,5v正(O2)= 4v逆(NO)
查看答案和解析>>
科目: 来源: 题型:
【题目】前四期元素A、B、C、D的原子序数依次增大,元素A核外电子有8种不同的运动状态;元素B的负一价离子的最外层电子数是次外层的4倍;元素C位于第四周期第ⅡA族;元素D最外层只有1个电子,次外层的所有原子轨道均充满电子。
(1)A原子核外有________种形状不同的原子轨道。
(2)与D同周期且同区的元素价层电子排布式为___________。
(3)上述四种元素中,第一电离能最小的是________________(填元素符号)。
(4) AB2的立体构型为___________,其中A的杂化方式为______________。
(5)A2的熔点比DA的___________(填“高”或“低”)。
(6) DA具有NaCl型结构,其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得DA的晶胞参数为α=480pm,则r(A2-)=________pm、r(D2+)=__________ pm。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属镍硬而有延展性并具有铁磁性,能够高度磨光和抗腐蚀。下图是一种以含镍废料(主要是NiO,含少量FeO、SiO2等杂质)制备Ni的流程:
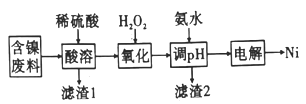
已知:室温下难溶物的溶度积数据如下表:
化合物 | Ni(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-15 | 10-15 | 10-38 |
(1)滤渣1的主要成分为_____________(填化学式)。
(2)实验中需用0.8mol/L的稀硫酸800mL,若用98%的浓硫酸(ρ=1.84g·mL-l)来配制,量取浓硫酸
时,需使用的量筒的规格为_________(填序号)。
A.10mL B.20mL C.50mL D.l00tnL
(3)用离子方程式解释加入H2O2的作用:_________________。
(4)滴加氨水调节至pH为_________时,铁刚好沉淀完全;若继续滴加氨水至pH为_____________时,镍开始沉淀(假定Ni2+浓度为0.lmol/L)。若上述过程中没有“氧化”步骤,其后果是_______________。
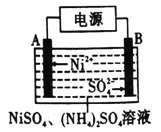
(5)电解制备镍的反应原理如图所示,则A电极的反应式为2H++2e-=H2↑和___________________。
(6)若用a kg含镍废料(含NiO 80%)制备Ni,最终得到产品b kg,则产率为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】N2O4是一种无色气体,常被用作火箭推进剂组分中的氧化剂。
(1)已知:①2O2(g)+N2(g)![]() N2O4(l) △H1;
N2O4(l) △H1;
②N2O4 (l)+O2(g)![]() N2(g)+2H2O(g) △H2;
N2(g)+2H2O(g) △H2;
联氨和从N2O4作为火箭推进剂时发生反应:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) 的△H=_________(用含△H1、△H2的式子表示)。
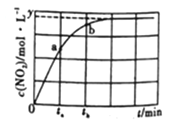
(2)一定温度下,在容积为2L的恒容密闭容器中充入xmolN2O4(g),发生反应:N2O4(g)![]() 2NO2(g) △H=+24.4kJ/mol。体系中NO2浓度随时间变化的情况如图所示。
2NO2(g) △H=+24.4kJ/mol。体系中NO2浓度随时间变化的情况如图所示。
①下列可作为判断反应达到平衡的依据是_______ (填序号)。
a.v正(N2O4)=2v逆(NO2). b.体系颜色不变
c.气体平均相对分子质量不变 d.气体密度不变
② ta时,v正_________v逆(填“>”“ =”或“<”,下同);ta时v逆____________tb时v逆。
③该反应的平衡常数K=__________。
④对于气体参与的反应,平衡常数也可用气体组分(B)的平衡分压p(B)代替该气体的平衡浓度c(B),
则该反应平衡常数KP=_____________ (用表达式表示);已知:上述反应中,正反应速率为v正=k正·p(N2O4),逆反应速率v逆= k逆·p2(NO2),其中k正、k逆为速率常数,则k正为_______________以k逆、KP表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子在指定溶液中一定能大量共存的是( )
A. 纯碱溶液中:Al3+、Ba2+、Cl-、NO3-
B. 室温下,pH=1的溶液中:K+、Fe2+、MnO4-、I-
C. 能使甲基橙变为黄色的溶液中:Na+、Al3+、Cl-
D. 室温下,![]() =1×10-12的溶液中:K+、Na+、CO32-、NO3-
=1×10-12的溶液中:K+、Na+、CO32-、NO3-
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活等多方面都密切相关,下列说法中不正确的是
A. 缺铁性贫血可以服用亚铁盐的药剂来进行治疗
B. 晶体硅制得的光电池,能将光能直接转化为电能
C. 误食重金属离子时可先喝大量牛奶或豆浆后再及时就医
D. 石油分馏可直接获得乙烯、丙烯和丁二烯等产品
查看答案和解析>>
科目: 来源: 题型:
【题目】阴离子Xn﹣含中子N个,X的质量数为A,则ag X的氢化物中含质子的物质的量是( )
A.![]() (N﹣a)mol
(N﹣a)mol
B.![]() (n+A)mol
(n+A)mol
C.![]() (N+n)mol
(N+n)mol
D.![]() (A﹣N+n)mol
(A﹣N+n)mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com