
科目: 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.将铜丝插入稀硝酸中:Cu+4H++2NO3-![]() Cu2++2NO2↑+H2O
Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe![]() 2Fe2+
2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O![]() Al(OH)3↓+3NH4+
Al(OH)3↓+3NH4+
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+![]() H2SiO3↓+2Na+
H2SiO3↓+2Na+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A. 风力、化石燃料、天然铀矿都是一次能源
B. 开发氢能、太阳能、风能、生物质能等新型能源是践行低碳生活的有效途径
C. 用脫硫处理的煤代替原煤作燃料可以有效减少空气中CO2气体的含量
D. 电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源
查看答案和解析>>
科目: 来源: 题型:
【题目】分子式为C4H7BrO2且能与碳酸氢钠反应生成气体的有机物数目,与下列各选项有机物数目相同的是(不含立体异构)
A. 分子式为C4H8O2的酯 B. 分子式为C5H10的烯烃
C. 甲苯的一氯代物 D. 立体烷( )的二氯代物
)的二氯代物
查看答案和解析>>
科目: 来源: 题型:
【题目】利用化学反应规律和原理,可以计算所得产物的质量。现有(NH4)2CO3和Ca(HCO3)2的混合物若干,进行下列反应。
(1)取a g该混合物溶于足量水中,写出反应的离子方程式_____________。
(2)取ag该混合物溶于足量水后,若生成沉淀的质量为m g,确定m的取值范围(用含有a的代数式表示,写出计算过程)_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】分别取40 mL的0.50 mol/L盐酸与40 mL0.55 mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
(1)理论上稀强酸、稀强碱反应生成1 mol水时放出57.3 kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式______________________________
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃棒,两个小孔不能开得过大,其原因是__________________;反应需要多次测量温度,每次测量温度后在进行下一次测量以前都必须采取的操作是____________________.
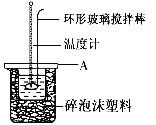
(3)假设盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容c=4.18 J/(g·℃).为了计算中和热,实验时还需测量的数据有(填序号)__________;
A.反应前盐酸溶液的温度 B.反应前盐酸溶液的质量 C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量 E.反应后混合溶液的最高温度 F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验 序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=____________;
(5)假定该学生的操作完全同上,实验中改用100 mL 0.5 mol/L盐酸跟100 mL 0.55 mol/L氢氧化钠溶液进行反应,与上述实验相比,所放出的热量_______(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”).
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下的定容容器中,当下列物理量不再发生变化时:
①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量
(1)能说明2SO2(g)+O2(g) ![]() 2SO3(g)达到平衡状态的是____________。
2SO3(g)达到平衡状态的是____________。
(2)能说明I2(g)+H2(g) ![]() 2HI(g)达到平衡状态的是_______________。
2HI(g)达到平衡状态的是_______________。
(3)能说明2NO2(g) ![]() N2O4(g)达到平衡状态的是______________________。
N2O4(g)达到平衡状态的是______________________。
(4)能说明C(s)+CO2(g) ![]() 2CO(g)达到平衡状态的是_________________。
2CO(g)达到平衡状态的是_________________。
(5)能说明NH2COONH4(s) ![]() 2NH3(g)+CO2(g)达到平衡状态的是__________。
2NH3(g)+CO2(g)达到平衡状态的是__________。
(6)能说明5CO(g)+I2O5(s) ![]() 5CO2(g)+I2(s)达到平衡状态的是________。
5CO2(g)+I2(s)达到平衡状态的是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,二氧化硫和氧气发生反应:2SO2(g)+O2(g) ![]() 2SO3(g)。
2SO3(g)。
(1)降低温度,化学反应速率________(填“增大”、“减小”、或“不变”)。
(2)600 ℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10 min和20 min时,分别改变了影响反应的一个条件,反应过程中SO2、O2、SO3物质的量变化如图所示,前10 min正反应速率逐渐____(填“增大”、“减小”或“不变”);前15 min内用SO3表示平均反应速率为________。
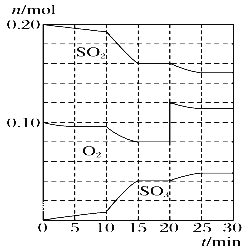
(3)图中反应进程,表示正反应速率与逆反应速率相等(即达到平衡状态)的时间段是_____________。
(4)根据如图判断,10 min时改变的条件可能是_______________________________(选填下面编号,下同);20 min时改变的反应条件可能是________。
a.加入催化剂 b.缩小容器容积
c.降低温度 d.增加O2的物质量
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液中通入SO2,其中SO2的作用与SO2使酸性KMnO4溶液褪色原理相同的是
A. 溴水溶液褪色B. 品红溶液褪色C. NaOH酚酞溶液褪色D. 石蕊溶液变红
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com