
科目: 来源: 题型:
【题目】燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点。下面是目前科学家正致力于研究的三种燃煤烟气脱硫和脱硝的方法。
(1)方法I:用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2 + H2O=(NH4)2SO3 (NH4)2SO4+ SO2 + H2O=2 NH4HSO3
①为了提高燃煤烟气中SO2去除率,可以采取的措施有:使燃煤烟气与氨水充分接触和______。
②燃煤烟气中含有大量的CO2,但在脱硫过程中,不需要先除去燃煤烟气的CO2原因是___________。
(2)方法II:用电化学原理将SO2转化为重要的化工原料H2SO4进行脱硫,装置如图所示。
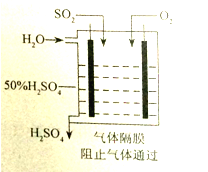
①写出通入SO2的电极的电极反应式:________。
②为使该脱硫过程稳定持续进行,硫酸溶液的浓度应维持不变,则通入的O2和加入的H2O的质量比为_________。
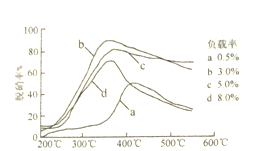
(3)方法Ⅲ:用乙烯作为还取剂将氨的氧化物还原为N2进行脱硝,其机理如图,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图所示。
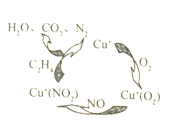
①写出该脱硝过程中乙烯和NO2反应的化学方程式:________________。
②如图,当负载率一定,达到某温度时脱硝率最高,而后却随着温度的升高脱硝率反而降低,其原因是__________;要达到最佳脱硝效果,应采取的条件是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:(1)Zn(s)+![]() O2(g)===ZnO(s) ΔH=-348.3 kJ·mol-1
O2(g)===ZnO(s) ΔH=-348.3 kJ·mol-1
(2)2Ag(s)+![]() O2(g)===Ag2O(s) ΔH=-31.0 kJ·mol-1
O2(g)===Ag2O(s) ΔH=-31.0 kJ·mol-1
则Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)的ΔH等于
A.-317.3 kJ·mol-1 B.-379.3 kJ·mol-1
C.-332.8 kJ·mol-1 D.317.3 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】aXn-和bYm+为两主族元素的离子,它们的电子层结构相同, 下列判断错误的是
A. 原子半径X<Y B. a+n=b-m
C. Y最高价氧化物的化学式为YOm D. X的氢化物的化学式为HnX
查看答案和解析>>
科目: 来源: 题型:
【题目】黄酮类化合物具有抗肿瘤活性,6-羟基黄酮衍生物的合成路线如下:
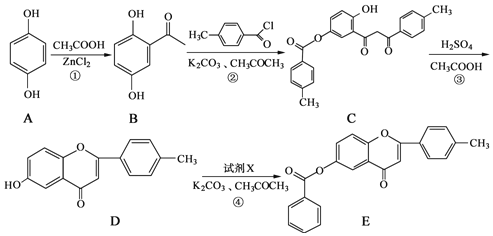
(1)化合物B中的含氧官能团的名称为_____和______。
(2)A→B的反应类型为___________。
(3)反应④中加入的试剂X的分子式为C7H5OCl,X的结构简式为________。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:__________。
①能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应;
②分子中有4种不同化学环境的氢。
(5)已知 请写出以
请写出以![]() 和CH3COOH为原料制备
和CH3COOH为原料制备
的合成路线流程图(无机试剂任选,合成路线流程图示例见本题题干)_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 2-甲基丁烷也称异丁烷
B. 由乙醇生成乙烯属于消去反应
C. C4H9Cl有3种同分异构体
D. 苯乙烯分子中的所有原子不可能处于同一平面
查看答案和解析>>
科目: 来源: 题型:
【题目】下列表示戊烷燃烧热的热化学方程式正确的是( )
A. C5H12(l)+8O2(g)![]() 5CO2(g) +6H2O(l) ΔH=-3 540 kJ·mol-1
5CO2(g) +6H2O(l) ΔH=-3 540 kJ·mol-1
B. C5H12(l)+8O2(g)![]() 5CO2(g)+6H2O(g) ΔH=-3 540 kJ·mol-1
5CO2(g)+6H2O(g) ΔH=-3 540 kJ·mol-1
C. C5H12(l)+8O2(g)![]() 5CO2(g)+6H2O(g) ΔH=+3 540 kJ·mol-1
5CO2(g)+6H2O(g) ΔH=+3 540 kJ·mol-1
D. C5H12(l)+8O2(g)![]() 5CO2(g)+6H2O(l) ΔH=+3 540 kJ·mol-1
5CO2(g)+6H2O(l) ΔH=+3 540 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面。工业上常以Ni(NO3) 6H2O和[CO(NH2)2](尿素)为原料制备。
(1)Ni2+基态核外电子排布式为_____________。
(2)与NO3-离子互为等电子体的一种分子的分子式为__________。
(3)尿素分子中碳原子轨道的杂化类型为________,1mol尿素分子中含有的σ键的数目为______。
(4)C、N、O三种元素第一电离能由大到小的顺序为_________。
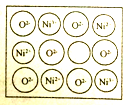
(5)NiO(氧化镍)晶体的结构与NaCl相同,但天然的和绝大部分人工制备体都存在各种缺陷,例如在某种NiO晶体中就存在如右图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。经测定某氧化镍样品中Ni3+与Ni2+的离子数之比为6:91,若该晶体的化学式为NixO,则x=________。
查看答案和解析>>
科目: 来源: 题型:
【题目】苹果酯是一种具有新鲜青苹果香味的日用香精,其合成线路如下图所示部分 产物已略去):
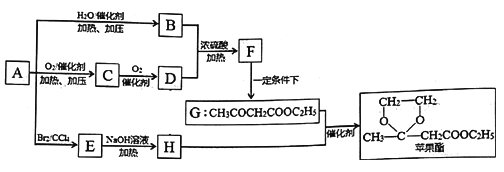
己知:i: 2mol F在一定条件下生成lmol G和lmol乙醇
ii:羰基化合物(醛或酮)与醇在一定条件下可以生成醚,如:
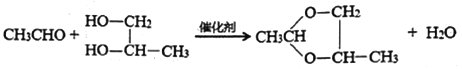
回答下列问题:
(1)F的分子式为 _________, 其名称为_________。
(2)A→B的化学方程式为______ ,其反应类型为__________。
(3)足量D与H反应的化学方程式为______________. 其反应类型为__________。
(4)N为F的酯类同分异构体,且能发生银镜反应,则N的结构简式可能为:__________。
(5)请以氯化苄(![]() )和H为起始原料,选用必要的无机试剂合成苯甲醛乙二醇缩醛(
)和H为起始原料,选用必要的无机试剂合成苯甲醛乙二醇缩醛(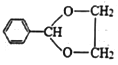 ),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________________
),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________________
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0mol/L的NaOH溶液240mL.一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤移液 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动
(1)配制溶液时,其正确的操作顺序为(填序号).本实验必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、、 .
(2)某同学欲称量NaOH的质量,先用托盘天平称量烧杯的质量,托盘天平平衡后的状态如图所示.烧杯的实际质量为g,要完成本实验该同学应称量g NaOH. 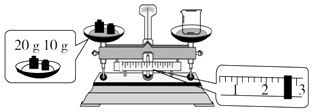
(3)使用容量瓶前必须进行的一步操作是 .
(4)配制过程中,下列操作会引起所配溶液浓度偏高的是(填序号).
A.转移溶液时,有少量溶液洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却至室温就将溶液移入容量瓶中并定容
D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加蒸馏水至刻度线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com