
科目: 来源: 题型:
【题目】可燃冰是一种天然气水合物,其主要成分为CH4nH2O,分布于深海沉积物或陆域的永久冻土中,下列有关说法正确的是( )
A. 可燃冰是一种清洁能源
B. CH4nH2O是一种离子化合物
C. 可燃冰在常温常压下能稳定存在
D. 可燃冰是天然气冷却后得到的固体
查看答案和解析>>
科目: 来源: 题型:
【题目】四氯化钛(TiCl4)是生产金属钛及其化合物的重要中间体。室温下,四氯化钛为无色液体。某化学兴趣小组同学以TiO2和CCl4为原料在实验室制取液态TiCl4,装置如图所示。

有关信息如下:
①反应原理:TiO2(s)+CCl4(g)![]() TiCl4(g)+CO2(g)。②反应条件:无水无氧且加热。
TiCl4(g)+CO2(g)。②反应条件:无水无氧且加热。
③有关物质性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它 |
CCl4 | 23 | 76 | 与TiCl4互溶 |
TiCl4 | 25 | 136 | 遇潮湿空气产生白雾 |
请回答下列问题:
(1)装置F橡皮管的作用是________________,装置F中有氮气生成,该反应的化学方程式为_______________。
(2)实验装置依次连接的顺序为F→B→_________________。
(3)实验开始前首先点燃____处酒精灯(填“D”或“F”),目的是___________________。
(4)E装置______(填“能”或“不能”)换成B装置,理由是______。
(5)欲分离C中的液态混合物,所采用操作的名称是__________________。
(6)TiCl4是制取航天航空工业材料——钛合金的重要原料。某钛合金的元素还有Al和Si等。已知在常温下,钛是一种耐强酸强碱的金属,请设计实验检验其中的铝元素: ___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
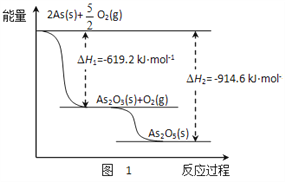
(1)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图1写出As2O5分解为As2O3的热化学方程式_________________。
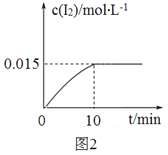
(2)砷酸钠具有氧化性,298 K时,在100 mL烧杯中加入10 mL 0.1 mol/L Na3AsO4溶液、20 mL 0.1 mol/L KI溶液和20 mL 0.05 mol/L硫酸溶液,发生下列反应:AsO43-(无色)+2I-+2H+![]() AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
①下列情况表明上述可逆反应达到平衡状态的是_______(填字母代号)。
a.溶液颜色保持不再变化 b.c(AsO33-)+c(AsO43-)不再变化
c.AsO43-的生成速率等于I2的生成速率 d. 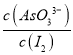 保持不再变化
保持不再变化
②0~10 min内,I的反应速率v(I)=_______。
③在该条件下,上述反应的平衡常数K=______。
④升高温度,溶液中AsO43-的平衡转化率减小,则该反应的 ΔH______0(填“大于”“小于”或“等于”)。
(3)利用(2)中反应可测定含As2O3和As2O5的试样中的各组分含量(所含杂质对测定无影响),过程如下:
①将试样0.2000 g溶于NaOH溶液,得到含AsO33-和AsO43-的混合溶液。
②上述混合液用0.02500 molL-1的I2溶液滴定,用____ 做指示剂进行滴定。重复滴定2次,平均消耗I2溶液40.00 mL。则试样中As2O5的质量分数是______。
(4)雄黄(As4S4)在空气中加热至300℃时会生成两种氧化物,其中一种氧化物为剧毒的砒霜(As2O3),另一种氧化物为______(填化学式),可用双氧水将As2O3氧化为H3AsO4而除去,写出该反应的化学方程式_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于动植物糖类、脂质的叙述中,正确的是
A. 核糖、葡萄糖、脱氧核糖是动植物体内共有的单糖
B. 葡萄糖、果糖、蔗糖均为还原性糖
C. 只有多糖、蛋白质、脂肪三类生物大分子以碳链为骨架
D. 固醇包括了脂肪、性激素、维生素D
查看答案和解析>>
科目: 来源: 题型:
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( ) 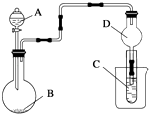
A.若A为浓盐酸,B为MnO2 , C中盛品红溶液,则C中溶液褪色
B.实验仪器D可以起到防止溶液倒吸的作用
C.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解
D.若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液不变浑浊
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物F(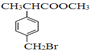 )是合成某种药物的中间体,它的一种合成路线如下:
)是合成某种药物的中间体,它的一种合成路线如下:

回答下列问题:
(1)A的结构简式为______,分子中处于同一平面的原子最多有____个。
(2)E中官能团名称是_____,①~④中属于加成反应的是_______(填序号)。
(3)反应③的化学方程式为______________。
(4)反应⑤的生成物有两种,除了F以外,另一种生成物的名称是______。
(5)满足下列条件的D的同分异构体有______种。
①能与FeCl3溶液发生显色反应; ②能发生银镜反应; ③分子中有1个甲基
(6)仿照E的合成路线,设计一种由![]() 合成
合成![]() 的合成路线_________________。
的合成路线_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:
2CH3OH(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
下列说法正确的是
A. 该反应的正反应为吸热反应
B. 容器I中反应达到平衡所需时间比容器Ⅲ中的长
C. 若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
D. 达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
查看答案和解析>>
科目: 来源: 题型:
【题目】向某密闭容器中加入0.6 mol A、0.2 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示(其中t0~t1阶段c(B)未画出)。t2时刻后改变条件反应体系中反应速率随时间变化的情况如图乙所示,且四个阶段都只改变一种条件并且改变的条件均不相同。下列说法正确的是
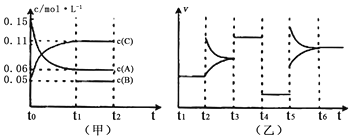
A. 反应的方程式为3A(g)+B(g)![]() 2C(g)
2C(g)
B. t3~t4,t4~t5,t5~t6各阶段改变的条件依次为:加催化剂,降低反应温度,增大压强
C. B的起始物质的量为0.08 mol
D. t0~t1阶段A的转化率为40%
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂用软锰矿(主要成分是MnO2,含少量Al2O3和SiO2)和闪锌矿(主要成分是ZnS,含少量FeS、CuS等杂质)为原料制备MnO2和Zn(干电池原料),其简化流程如下:

已知:反应Ⅰ中所有金属元素均以离子形式存在。
回答下列问题:
(1)滤渣1中除了SiO2以外,还有一种淡黄色物质,该物质是由MnO2、CuS与硫酸共热时产生的,请写出该反应的离子方程式________________________________。
(2)反应Ⅱ中加入适量金属锌的目的是为了回收某种金属,滤渣2的主要成分是______(填名称)。
(3)反应Ⅲ中MnO2的作用是______,另外一种物质X可以是______。(填字母代号)
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(4)反应Ⅳ中电极均是惰性电极,写出阳极电极反应式_______________。本工艺可以循环利用的物质有MnO2、Zn和_____。
(5)已知:H2S的电离常数K1=1.0×107,K2=7.0×1015。0.1 mol/L NaHS的pH___7(填“>”“=”或“<”),理由是________________________________________。
(6)在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L1 Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS浓度为1.0×104 mol·L1时,Mn2+开始沉淀,则a=________。[已知:Ksp(MnS)=1.4×1015]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com