
科目: 来源: 题型:
【题目】利用铜—氯热化学循环可制取氢气,主要流程如下:
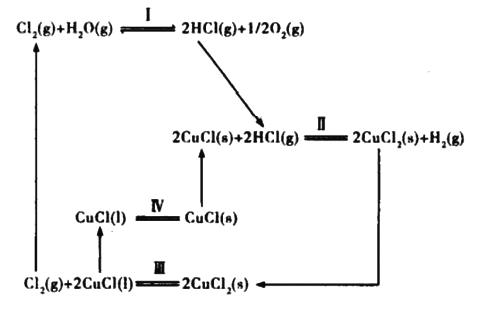
回答下列问题:
(1)图中属于氧化还原反应的是__________(填序号)。
(2)已知25℃时,Ksp(CuOH)=2.0×10-15,Ksp(CuC1)=1.0×10-6,则反应CuC1(s)+H2O(1)![]() CuOH(s)+Cl-(aq)+H+(aq)的平衡常数K=___________(填数值)。
CuOH(s)+Cl-(aq)+H+(aq)的平衡常数K=___________(填数值)。
(3)已知:
Cl2(g)+H2O(g)==2HCl(g)+1/2O2(g) △H1
2CuCl(s)+2HCl(g)==2CuCl2(s)+H2(g) △H2
Cl2(g)+2CuCl(l)==2CuCl2(s) △H3
CuC1(l)==CuC1(s) △H4
则反应H2O(g)==H2(g)+1/2O2(g) △H=_______(用△H1、△H2、△H3、△H4表示)。
(4)反应Ⅱ若在水溶液中进行可用惰性电极电解实现,其装置如下图所示。阳极的电极反应式为____________________;电解过程中阳极周围溶液的pH__________(填“升高”或“降低”)。

(5)反应I是可逆反应,工业上也常用该反应生成的HC1制取氯气,反应为4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g),在不同起始投料比m下,HC1平衡转化率随温度的变化关系如下图所示:
2Cl2(g)+2H2O(g),在不同起始投料比m下,HC1平衡转化率随温度的变化关系如下图所示:
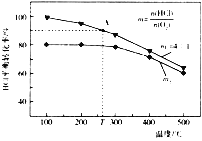
①该反应的正反应为___________热反应(填“放”或“吸”)。
②图中m2________m1(填“>”或“<”)。
③p kPa下,A点对应温度下反应的平衡常数Kp=________kPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】《太平惠民和剂局方》中对精制蜡的过程有如下记载:“……先将蜡六两熔化作汁,以重绵滤去滓,以好酒一升,于银石器内煮蜡熔,数沸倾出,候酒冷,其蜡自浮,取蜡称用。”文中涉及的操作方法是( )
A. 萃取B. 升华C. 重结晶D. 渗析
查看答案和解析>>
科目: 来源: 题型:
【题目】砷及其化合物广泛用于制造半导体材料以及用于医疗、农药等。回答下列问题:
(1)砷与氮同主族,原子序数比氮大26,则砷在元素周期表中的位置是____________;砷化氢的电子式为______________________。
(2)H3AsO3又叫路易斯酸,是一种弱酸,发生酸式电离是通过和水中的氢氧根离子结合实现的,则第一步电离方程式为____________________________________________;若常温时H3AsO3的第一步电离常数Ka1=1.0×10-9,则常温下,0.1mol·L-1的H3AsO3溶液的pH为_______________。
(3)利用可逆的氧化还原反应AsO![]() +2I-+2H+
+2I-+2H+![]() AsO
AsO![]() +I2+H2O可以设计为原电池,起始时在甲、乙两池中分别加入图示药品并连接装置。
+I2+H2O可以设计为原电池,起始时在甲、乙两池中分别加入图示药品并连接装置。
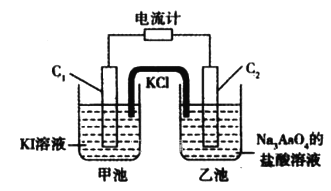
①起始时,甲池石墨棒C1上发生的电极反应为_____________________。
②一段时间后指针不发生偏转。欲使指针偏转方向与起始时相反,应采取的可行措施是_______________________________________________________________(举一例)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关乙炔性质的叙述中,既不同于乙烯又不同于乙烷的是( )
A. 能燃烧生成CO2和H2O
B. 能发生加成反应
C. 能与KMnO4发生反应
D. 能与HCl反应生成氯乙烯
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A. 14g乙烯和丙烯混合气体中的氢原子数为2NA
B. 27g铝中加入1mol/L的NaOH溶液,转移电子数是3NA
C. 1 molFe溶于过量硝酸,电子转移数为2NA
D. 标准状况下,44. 8LNO与22. 4LO2反应后的分子数是2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】如表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )
选项 | X | Y | Z | 箭头上所标数字的反应条件 |
A | Na2O2 | NaOH | NaCl | ①常温遇水 |
B | Al2O3 | NaAl(OH)4 | Al(OH)3 | ②通入CO2 |
C | NO | NO2 | HNO3 | ④加入铜粉 |
D | C | CO | CO2 | ③点燃镁条 |
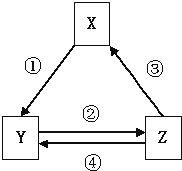
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】三氯化磷是一种无色液体,熔点-93.6℃,沸点76.1℃,PCl3遇到水蒸气剧烈反应。实验室利用下列装置制备三氯化磷。

(1)仪器W的名称是______________,其作用是______________________________。
(2)盛P2O5的长玻璃管的作用是___________,浓硫酸的作用是_____。
(3)实验室用KMnO4与浓盐酸制取氯气的离子方程式为________________________。
(4)氯气通入烧瓶中会发生燃烧,说明P4与Cl2反应的△H____0(填“>”或“<”)。
(5)烧瓶中得到的产物除PCl3外还可能含有______(填化学式),进一步精制的方法是________。
(6)PCl3与H2O反应的化学方程式为________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物H是一种香料,其合成路线如下:
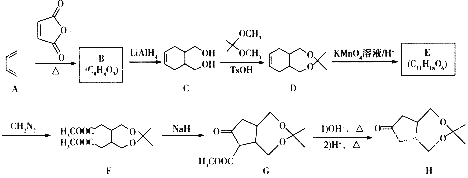
回答下列问题:
(1)A的化学名称为____________,H中含氧官能团名称是________________。
(2)A生成B的反应类型是____________,C生成D的反应类型是____________。
(3)B的结构简式为____________,E的结构简式为____________。
(4)F与足量NaOH溶液反应的化学方程式为________________________________。
(5)芳香化合物X是G的同分异构体,X与金属钠不反应,其核磁共振氢谱显示有4种不同化学环境的氢,写出1种符合要求的X的结构简式:____________________。
(6)写出以1,2-二氯环戊烷和丙烯酸甲酯为原料制备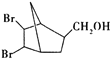 的合成路线:________________________________(其他试剂任选)。
的合成路线:________________________________(其他试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒容密闭容器中通入X并发生反应:2X(g)![]() Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是
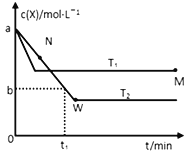
A. 该反应进行到M点放出的热量大于进行到W点放出的热量
B. T2下,在0~t1时间内,υ(Y)=a-b/t1 mol/(L·min)
C. M点的正反应速率υ(正)大于N点的逆反应速率υ(逆)
D. M点时再加入一定量的X,平衡后X的转化率减小
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机物性质的叙述不正确的是
A. 大多数有机物难溶于水,易溶于有机溶剂
B. 有机物参加的反应比较复杂,一般情况下反应较慢
C. 有机物一般硬度大、熔点高
D. 绝大多数有机物受热易分解,容易燃烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com