
科目: 来源: 题型:
【题目】海藻中含有丰富的、以碘离子形式存在的碘元素.在实验室中,从海藻里提取碘的流程和实验装置如下: 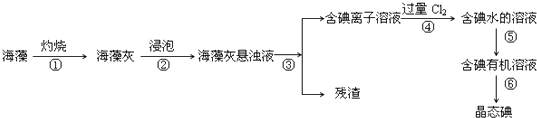
(1)写出步骤④对应反应的离子方程式: .
(2)步骤④除了加入过量Cl2 , 下列氧化剂最好选用(填代号).
A.浓硫酸 B.H2O2溶液 C.KMnO4溶液
理由是 .
(3)步骤⑤中,某学生选择用苯提取碘的理由是 .
(4)设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A. 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物
B. 碘晶体受热转变成碘蒸气,破坏了共价键
C. CH3CH2OH和CH3OCH3互为同分异构体
D. 加热氧化镁使之熔化克服的是共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】如表标出的是元素周期表的一部分元素,回答下列问题:
1 | A | |||||||||||||||||
2 | B | |||||||||||||||||
3 | C | D | E | F | G | H | I | |||||||||||
4 | J | K | ||||||||||||||||
5 | ||||||||||||||||||
6 | ||||||||||||||||||
(1)表中用字母标出的元素中,化学性质最不活泼的是(用元素符号表示,下同),其原子结构示意图为 .
(2)表中用字母标出的元素中,能形成两性氢氧化物的元素是(用元素符号表示),写出该元素的单质与C最高价氧化物的水化物反应的化学方程式 .
(3)在C、D、E形成的氢氧化物中,碱性最强的是(用化学式表示);在F、G、H形成的氢化物中最稳定的是(用化学式表示).
(4)A和B可形成最简单的有机化合物,其结构式为;它的空间构型是 .
(5)在H、K对应的单质中,氧化性较弱的是(用化学式表示).
(6)J元素是过渡元素铁,工业上常用赤铁矿(主要成分为Fe2O3)为原料,采用高炉炼铁的方式炼铁,其原理是,把赤铁矿、焦碳和石灰石一起加入高炉,在高温下,把铁从赤铁矿中还原出来,写出该反应的化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】由于燃料电池汽车,尤其氢燃料电池汽车可以实现零污染排放,驱动系统几乎无噪音,且氢能取之不尽、用之不竭,燃料电池汽车成为近年来汽车企业关注的焦点。为了获得竞争优势,各国纷纷出台政策,加速推进燃料电池关键技术的研发。燃料电池的燃料选择有氢气、甲醇等。
(1)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气合成为甲醇,甲醇是汽车燃料电池的重要燃料。已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2(g)=2H2O(1) △H=-285kJ/mol ①
CH3OH(l)十![]() O2(g)=CO2(g)+2H2O(1) △H=-726.0 kJ/mol ②
O2(g)=CO2(g)+2H2O(1) △H=-726.0 kJ/mol ②
写出二氧化碳与氢气合成甲醇液体的热化学方程式:________________。
(2)有科技工作者利用稀土金属氧化物作为固体电解质制造出了甲醇-空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。
①这个电池的负极发生的反应是_____________。
②在稀土氧化物的固体电解质中,O2-的移动方向是_____________。
③甲醇可以在内燃机中燃烧直接产生动力推动机动车运行,而科技工作者要花费大量的精力研究甲醇燃料汽车,主要原因是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳和氮的单质及其化合物在工农业生产和生活中有重要的作用。用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO (g)![]() N2(g)+CO2(g) △H= QkJ/mol。
N2(g)+CO2(g) △H= QkJ/mol。
在T1℃时,反应进行到不同时间测得各物质的浓度如下:

(1)0~10min内,NO的平均反应速率V(NO)=______,T1℃,该反应的平衡常数K=________;
(2) 30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是______.(填字母编号)。
a.通入一定量的NO b.加入一定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
(3)若30 min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q_____0(填“>”或“<")。
(4)在恒容条件下,能判断该反应一定达到化学平衡状态的依据是______(填选项编号)。
a.单位时间内生成2nmol NO (g)的同时消耗nmol CO2(g) b.反应体系的温度不再发生改变
c.混合气体的密度不再发生改变 d.反应体系的压强不再发生改变
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质中均属于蛋白质类物质的一组是( )
①胰岛素 ②雌性激素 ③抗体 ④运输载体 ⑤维生素D
A. ①②③ B. ①③⑤ C. ①④⑤ D. ①③④
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关中和滴定的操作:①用标准液润洗滴定管;②往滴定管内注入标准溶液;③检查滴定管是否漏水;④滴定;⑤滴加指示剂于待测液;⑥用水洗涤。正确的操作顺序是( )
A.⑤④③②①⑥B.⑤①②⑥④③
C.③⑥①②⑤④D.③①②④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】对下列物质溶于水时破坏的作用力描述错误的是
A. 氯化钠,破坏了离子键B. 氯化氢,破坏了共价键
C. 蔗糖,破坏了分子间作用力D. 二氧化碳,没有破坏作用力
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com