
科目: 来源: 题型:
【题目】已知温度T时水的离子积常数为Kw,该温度下,将浓度为amol/L的一元酸HA与bmol/L的一元碱BOH等体积混合,可判断该溶液呈中性的依据是:
A. a=b
B. 混合溶液的pH值为7
C. 混合溶液中C(H+)=![]()
D. 混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
查看答案和解析>>
科目: 来源: 题型:
【题目】【2017金凤区校级三模】一定的条件下,合成氨反应为:N2(g)+3H2(g)2NH3(g).图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线.图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.
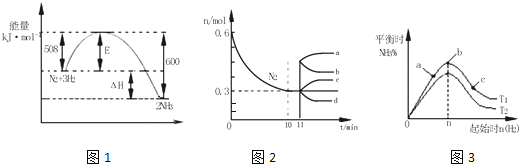
①由图2信息,计算0~10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为 ;
②图3a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于氮及其化合物的说法错误的是( )
A. N2化学性质稳定,是因为分子内氮氮键很强
B. NO、NO2均为大气污染气体,在大气中可稳定存在
C. 可用浓盐酸检测输送NH3的管道是否发生泄漏
D. HNO3具有强氧化性,可溶解铜、银等不活泼金属
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是
A. 4g重水(D2O)中所含质子数为0.2NA
B. 4.48L N2与CO的混合物所含分子数为0.2NA
C. 6.2g白磷与红磷的混合物中所含磷原子数为0.2NA
D. 12.5mL 16mol·L-1浓硫酸与足量铜反应,转移电子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】用惰性电极电解下列溶液,一段时间后(原溶液溶质未完全反应),再加入一定质量的另一物质(中括号内),溶液能与原来溶液完全一样的是 ( )
A.CuCl2[CuCl2溶液]B.AgNO3[Ag2O]
C.NaCl[HCl溶液]D.CuSO4[Cu(OH)2]
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A. Na2O2用作呼吸面具的供氧剂B. NaHCO3的热稳定性大于Na2CO3
C. 乙醇可与金属钠反应放出氢气D. 钠久置在空气中最终产物为Na2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制备硝基苯的反应原理和实验装置如下: ![]()
存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯,有关数据如表:
物质 | 熔点/℃ | 沸点/℃ | 密度/gcm﹣3 | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
浓硝酸 | 83 | 1.4 | 易溶于水 | |
浓硫酸 | 338 | 1.84 | 易溶于水 |
实验步骤如下:
取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混合液,将混合酸小心加入B中,把17.73mL(15.6g)苯加入A中.向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀,在50~60℃下发生反应,直至反应结束.
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5% NaOH溶液和水洗涤.分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2 , 进行蒸馏纯化,收集205~210℃馏分,得到纯硝酸基苯18.45g.回答下列问题: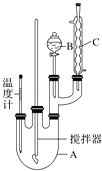
(1)装置B的名称是 , 装置C的作用是;
(2)配制混合液时,(填“能”或“不能”)将浓硝酸加入到浓硫酸中,说明理由:;
(3)为了使反应在50~60℃下进行,常用的方法是;
(4)在洗涤操作中,第二次水洗的作用是;
(5)本实验所得到的硝基苯产率是(保留两位有效数字).
查看答案和解析>>
科目: 来源: 题型:
【题目】【2016·南京高三调研】一定条件下,对于可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
A.c1∶c2=1∶3
B.平衡时,Y和Z的生成速率之比为2∶3
C.X、Y的转化率不相等
D.c1的取值范围为0 mol·L-1<c1<0.14 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下0.1molC12溶于水,转移的电子数目为0.1NA
B. 1 L 0.1 molL-1氯化铁溶液中铁离子数为0.1NA
C. 0.1 molNa2O2与足量的潮湿的二氧化碳反应转移的电子数为0.1NA
D. 标准状况下,2.24LNO和2.24LO2混合后气体分子数一定为0.15NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com