
科目: 来源: 题型:
【题目】布洛芬常来减轻感冒症状,其结构简式如图,下列有关说法正确的是( )
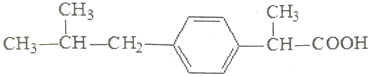
A. 布洛芬的分子式为C13H17O2 B. 布洛芬在核磁共振氢谱中呈现出10种峰
C. 布洛芬与苯乙酸是同系物 D. 布洛芬在苯环上发生取代反应,其一氯代物存4种
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)水的电离平衡曲线如下图所示。
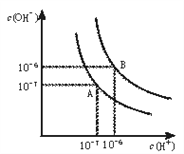
将100℃下的pH=8的Ba(OH)2溶液与100℃下的pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=7, 则Ba(OH)2与盐酸的体积比为______________
(2)下列关于水电离的说法正确的是(____)
A.水电离是熵增加的反应,反应吸热,故能自发进行
B.升高温度水分子的活化分子数增多,有效碰撞几率减小,电离速率加快
C.向水中加入多电子体,加快H+和O2-之间的电子传递, 破坏水的电离平衡,是研究水分解的方向之一
D.水电离本质上是水分子间的氢键瞬间作用力加强造成的
查看答案和解析>>
科目: 来源: 题型:
【题目】50mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液在图所示的装置 中进行中和反应,通过测定反应过程中所放出的热量可计算反应热. 
(1)烧杯间填满泡沫塑料的作用是;
(2)大烧杯上若不盖硬纸板,求得的中和热数值(填“偏大”、“偏小”、“无影响”)
(3)如上图所示,仪器A的名称是;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H﹣57.3KJ/mol(填“>”、“<”或“=”);
(4)实验中改用80mL 0.50mol/L盐酸跟100mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等、“不相等”),所求中和热(填“相等、“不相等”).
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会;(均填“偏大”、“偏小”、“无影响”)
(6)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。

(1)写出单质B与强碱溶液反应的离子方程式___________________________,写出由沉淀J生成H溶液的离子方程式_______________________________。
(2)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式______________________________。
(3) K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:_______________
(4)溶液I中所含金属离子是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究NOx、CO2的吸收利用对促进低碳社会的构建和环境保护具有重要意义。
(1)已知:① 2H2(g) + O2(g)=2H2O(g) H1
② CO2(g)+3H2(g)![]() CH3OH (l) + H2O (l) H2
CH3OH (l) + H2O (l) H2
③ H2O(g)![]() H2O(l) H3
H2O(l) H3
求 25℃、101kPa下,2 mol CH3OH (l)完全燃烧的H=_____(用含H1、H2、H3的式子表示)。
(2)向1 L密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) ![]() CH3OH (l) + H2O (l) H2
CH3OH (l) + H2O (l) H2
①已知反应的H2<0,则此反应自发进行的条件是_________(填“低温”、“高温”或“任意温度”)。
②在t2时将容器容积缩小为原体积的一半,t3时再次达到平衡,请画出t2之后 CO2气体的浓度随时间变化的曲线。______________

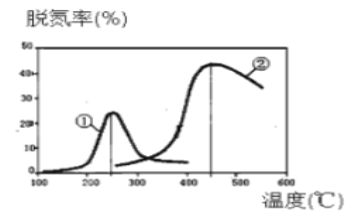
(3)用NH3催化还原NOX可以消除氮氧化物的污染。如下图,采用NH3作还原剂,烟气以一
定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为:NO(g) + NO2(g) + 2NH3(g)![]() 2N2(g) + 3H2O(g)。 以下说法不正确的是__________。(填编号)
2N2(g) + 3H2O(g)。 以下说法不正确的是__________。(填编号)
A.使用第②种催化剂更有利于提高NOx的平衡转化率
B.催化剂①、②分别适合于250℃和450℃左右脱氮
C.相同条件下,改变压强对脱氮率会有影响
D.烟气通过催化剂的流速越快,脱氮效果会越好
(4)用电解法处理NO2是消除氮氧化物污染的新方法,其原理是将NO2在电解池中分解成无污染的N2和O2,电解质是固体氧化物陶瓷(内含O2ˉ离子,可定向移动),阳极的反应式是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列电离方程式正确的是( )
A. 醋酸溶于水:CH3COOH===CH3COO-+H+
B. NaHSO4溶于水:NaHSO4===Na++HSO4-
C. 碳酸氢钠溶于水:NaHCO3![]() HCO
HCO![]() +Na+
+Na+
D. 次氯酸溶于水:HClO![]() H++ClO-
H++ClO-
查看答案和解析>>
科目: 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH- ΔH>0。下列叙述正确的是( )
H++OH- ΔH>0。下列叙述正确的是( )
A. 将水加热,Kw增大,pH不变
B. 向水中加入少量NaOH溶液,平衡逆向移动,c(OH-)减小
C. 向水中加入少量冰醋酸,平衡正向移动,c(H+)增大
D. 向水中加入少量固体NaHSO4,c(H+)增大,Kw不变
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组欲制备漂白剂亚氯酸钠(NaClO2)。甲同学通过查阅文献发现:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体的是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
实验I 乙同学利用下图所示装置制取NaClO2晶体

(l)装置B中生成了ClO2,反应的化学方程式为_________________________________。
(2)装置A和E的作用是_____________________。
(3)装置D中发生反应的化学方程式为_________________________________________。
(4)反应结束后,先将装置D反应后的溶液在55℃条件下减压蒸发结晶,然后进行的操作是_________________,再用38℃~60℃的温水洗涤,最后在低于60℃条件下干燥,得到NaClO2晶体。
实验Ⅱ 丙同学设计实验测定制得NaClO2样品的纯度
其实验步骤如下:
① 称取所得亚氯酸钠样品ag于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应后,配成100mL混合液。
② 取25.00 mL待测液于锥形瓶中,用bmol/LNa2S2O3标准液滴定,消耗标准液体积的平均值为VmL(已知:I2+2S2O32-=2I-+S4O62-)。
(5)步骤① 反应的离子方程式为__________________________________________。
(6)步骤② 滴定中使用的指示剂是____________________。
(7)样品中NaClO2的质最分数为_________________(用含a、b、V的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】对细胞中的某些物质的组成进行分析,可以作为鉴别真核生物的不同个体是否为同一物种的辅助手段,一般不采用的物质是( )
A. 蛋白质 B. DNA C. RNA D. 核苷酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com