
科目: 来源: 题型:
【题目】取500.0mL Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到6.27g白色沉淀,用过量稀硝酸处理后沉淀量减少到2.33g,并有气体放出.试计算:
(1)原混合溶液中Na2CO3和Na2SO4的物质的量浓度分别为 , ;
(2)产生的气体在标准状况下的体积 .
查看答案和解析>>
科目: 来源: 题型:
【题目】某科研小组利用工业废料(主要成分NiO,含有少量Al2O3、FeO、CuO、BaO)回收NiO,并制备其他部分产品的工艺流程如下:

已知:①溶液中离子浓度小于等于1.0×10-5 mol·L-1时,认为该离子沉淀完全。
②25℃时,部分难溶物的溶度积常数如下表所示:
难溶物 | CuS | Al(OH)3 | Ni(OH)2 | Fe(OH)3 | Fe(OH)2 |
溶度积常数(Ksp) | 6.3×10-36 | 1.3×10-33 | 2.0×10-15 | 4.0×10-38 | 1.8×10-16 |
请回答下列问题:
(1)H2S的电子式为_______________________________。
(2)“酸浸”时,Ni的浸出率与温度的关系如图所示。 温度高于70℃,Ni的浸出率降低的主要原因为___________________________________________________________。
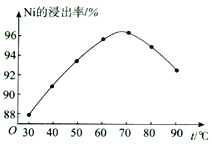
(3)“沉淀1”的主要成分为____________________(填化学式)。
(4)“滤液1”中通入H2S的作用为___________________。
(5)“转化”过程中,发生反应的主要离子方程式为________________________________。
(6)25℃时,“调节pH2”使沉淀3中金属阳离子沉淀完全后,所得溶液中的C(H+)最大为____________(保留三位有效数字,已知![]() ≈1.4)。
≈1.4)。
(7)“操作I”主要包括蒸发浓缩、__________________、过滤、洗涤、干燥。
(8)NiO可通过铝热反应冶炼Ni,该反应的化学方程式为________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】SO2和CO均为燃煤烟气中的主要污染物,对二者的治理备受瞩目。
请回答下列问题:
(1)下列事实中,不能用于比较硫元素和碳元素非金属性强弱的是___________(填选项字母)。
A.SO2能使酸性KMnO4溶液褪色而CO2不能
B.相同条件下,硫酸的酸性强于碳酸
C.CS2中硫元素显-2价
D.相同条件下,SO3的沸点高于CO2
(2)有人设计通过硫循环完成二者的综合处理,原理为
i.2CO(g) +SO2 (g)![]() S(l)+2CO2(g) △H1=-37.0 kJ·mol-1
S(l)+2CO2(g) △H1=-37.0 kJ·mol-1
ii.S(l) + 2H2O(g)![]() 2H2(g) + SO2(g) △H2 =-45.4 kJ·mol-1
2H2(g) + SO2(g) △H2 =-45.4 kJ·mol-1
1 mol CO和水蒸气完全反应生成H2和CO2的热化学方程式为__________________________。
(3)T℃,向5L恒容密闭容器中充入2 mol CO和1 mol SO2,发生反应i。10min达到平衡时,测得S(l)的物质的量为0.8mol。
①010 min内,用CO表示该反应速率v(CO)=____________________。
②反应的平衡常数为______________________。
(4)起始向密闭容器中充入一定量的S(1)和H2O(g),发生反应ii。H2O(g)的平衡转化率与温度(T)和压强(p)的关系如图所示。
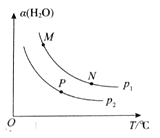
①M、P两点的平衡转化率:a(M)___________a(P)(填“>”“<”或“=”),理由为_____________________。
②N、P两点的平衡常数:K(N)___________K(P)(填“>”“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 增大压强,活化分子百分数增大,化学反应速率一定增大
B. 升高温度,活化分子百分数增大,化学反应速率可能增大
C. 加入反应物,使活化分子百分数增大,化学反应速率增大
D. 一般使用催化剂可以降低反应活化能,增大活化分子百分数,增大化学反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、N5+等已被发现。下列有关说法中正确的是
A. O2与O4属于同位素 B. H2与H3属于同素异形体
C. C60的相对分子质量为720g/mol D. N5+中含有36个电子
查看答案和解析>>
科目: 来源: 题型:
【题目】在反应KMnO4+HCl(浓)→MnCl2+KCl+Cl2↑+H2O中,
(1)配平上述化学方程式
(2)若生成35.5g Cl2 , 则被氧化的HCl是mol,转移的电子的物质的量是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在25℃,101kPa下,lgC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是( )
A. C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(g) △H=-48.40kJ·mol-1
B. C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(1) △H=-5518kJ·mol-1
C. C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(1) △H=+5518kJ·mol-1
D. C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(1) △H=-48.40kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:25℃时,氨水的电离常数Kb(NH3·H2O) = 1.8×10-5。该温度下,用0.1 mol·L-1的氨水滴定10.00 mL 0.1 mol·L-1的HA溶液,溶液的pH与所加氨水的体积(V)的关系如图所示。下列说法正确的是( )
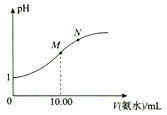
A. HA为弱酸
B. M点溶液中存在c(A-)=c(NH4+)+c(NH3·H2O)
C. M、N两点溶液中水电离出来的c(H+):M<N
D. 25℃时,NH4+的水解平衡常数为1.8×10-9
查看答案和解析>>
科目: 来源: 题型:
【题目】蔗糖与不同浓度的硫酸可发生:①水解反应;②脱水反应;③加成反应;④取代反应;⑤加聚反应。正确的是( )
A. ①② B. ③④
C. ③⑤ D. ③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示反应A(g)+B(g)![]() n C(g);(正反应为放热反应),在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述正确的是( )
n C(g);(正反应为放热反应),在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述正确的是( )
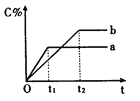
A. 反应由逆反应开始
B. a表示有催化剂,b表示无催化剂
C. 若n=2,其它条件相同,a比b的压强大
D. 若其它条件相同,a比b的温度高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com