
科目: 来源: 题型:
【题目】物质的量浓度相同的三种一元酸的钠盐NaX、NaY、NaZ溶液的pH 分别为8、9、10,则这三种一元酸的酸性由强到弱的顺序为
A. HX>HY>HZ B. HX>HZ>HY
C. HZ>HY>HX D. HY >HX>HZ
查看答案和解析>>
科目: 来源: 题型:
【题目】相同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液的体积比是6:3:2,则三种溶液中氯离子的物质的量浓度之比为
A. 1:1:1 B. 3:2:1 C. 1:2:3 D. 6:3:2
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用密度为1.25gmL﹣1 , 溶质质量分数为36.5%的浓盐酸配制 240mL 0.1molL﹣1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为 .
(2)配制240mL 0.1molL﹣1的盐酸
应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) . A.用30mL水洗涤2~3次,洗涤液均注入容量瓶,振荡
B.用准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡、摇匀
E.改用加水,使溶液凹液面最低处恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线处
(4)操作A中,将洗涤液都移入容量瓶,其目的是
(5)若实验过程中出现如下情况如何处理? ①加蒸馏水时不慎超过了刻度线: .
②向容量瓶中转移溶液时不慎有液滴溅在容量瓶外面: .
(6)若实验遇到下列情况,溶液的浓度是偏高,偏低还是不变? A.定容时仰视刻度线;
B.忘记将洗涤液加入容量瓶;
C.容量瓶内壁附有水珠而未干燥处理;
D.溶解后没有冷却便进行定容 .
查看答案和解析>>
科目: 来源: 题型:
【题目】今有五种有机物:①CH2OH(CHOH)4CHO,②CH3(CH2)3OH,③CH3=CH—CH2OH,④CH2=CH—COOCH3,⑤CH2=CH—COOH。其中既能发生加成反应、加聚反应、酯化反应,又能发生氧化反应的是
A. ③⑤ B. ①②⑤ C. ②④ D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】A一J是中学化学中常见的物质,其相互转化关系如下图所示,反应条件均已略去。A、B常温下均为无色液体,且均由两种相同的元素组成;C、F、G均为非金属单质,常温下C、F为无色气体,G可用于制取“84”消毒液;D是应用最广泛的金属;J溶液中滴入KSCN 溶液显红色。
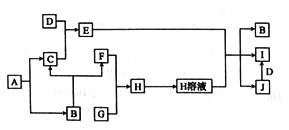
回答下列问题:
(1)A的化学式是_________,E 的俗称是_______。
(2)在空气中点燃F,然后把导管缓缓伸入盛满G的集气瓶中,观察到的实验现象是______。
(3)B和G能发生反应,写出反应的离子方程式______。
(4)G和I能发生反应,写出反应的化学方程式,并标出电子转移的方向和数目:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。

请回答下列问题:
(1)B的化学式为________。
(2)反应②在工业上通常称之为________工业。
(3)写出反应③的离子方程式___________________________。
(4)写出反应④的化学方程式____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室常用以下方法制取氯气:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用.请你根据所学知识回答
MnCl2+Cl2↑+2H2O,氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用.请你根据所学知识回答 
下列问题:
(1)把氯气通入紫色石蕊试液中,可以观察到的现象是: . 请你解释其中的原因 .
(2)若上述反应产生的氯气在标准状况下的体积为11.2L.试计算:参加反应的MnO2的质量?
(3)为保证实验安全,常用NaOH溶液吸收多余的氯气.当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2molL﹣1的NaOH溶液的体积至少应为多少?(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】镁铝合金在工业上有着广泛的用途,氧化铝是冶炼金属铝的主要原料。从铝土矿(主要成分是Al2O3,含有SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:

回答下列问题:
(1)Al2O3、SiO2、Fe2O3、MgO四种物质中,属于酸性氧化物的是______,属于碱性氧化物的是______。
(2)流程一中,沉淀③是_________(填化学式,下同),沉淀⑥是_________。
(3)流程二中,加入烧碱溶解SiO2的化学方程式为_________。
(4)滤液⑤中的可溶性盐是NaCl、______(填化学式),滤液⑨与过量氨水反应的离子方程式为_____。
(5)在电解氧化铝制取金属铝的反应中,氧化产物与还原产物的质量之比为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知醋酸达到电离平衡后,改变某条件平衡向电离方向移动,则下列说法正确的是
A. 实现该变化的只能是升高温度
B. 溶液的导电能力一定变强
C. 溶液的pH一定减小
D. 发生电离的分子总数增多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com