
科目: 来源: 题型:
【题目】硼是植物生长发育必需的微量元素之一,硼玻璃纤维用作火箭的防护材料。下列关于硼的叙述正确的是
A. 硼原子的L电子层中有2个电子 B. 硼酸是弱酸
C. 硼的金属性比铝的金属性强 D. 硼的原子半径比碳的原子半径小
查看答案和解析>>
科目: 来源: 题型:
【题目】某烃完全燃烧时,消耗的氧气与生成的CO2体积比为3∶2,该烃能使酸性高锰酸钾溶液褪色,也能使溴水褪色,则该烃的分子式可能为
A. C3H4 B. C2H4 C. C2H6 D. C6H6
查看答案和解析>>
科目: 来源: 题型:
【题目】实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为:
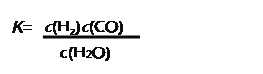 它所对应的化学反应为:__________
它所对应的化学反应为:__________
(2)已知在400℃时,N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正_____v(N2)逆(填:>、<、=、不能确定);欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积分数增加,
2NH3(g) ΔH<0的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正_____v(N2)逆(填:>、<、=、不能确定);欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积分数增加,
可采取的正确措施是____________(填序号)
A. 缩小体积增大压强 B.升高温度 C.加催化剂 D.使氨气液化移走
(3)在一定体积的密闭容器中,进行如下化学反应:
A(g)+3B(g) ![]() 2C(g)+D(s) ΔH,其化学平衡常数K与温度t的关系如下表:
2C(g)+D(s) ΔH,其化学平衡常数K与温度t的关系如下表:
t/K | 300 | 400 | 500 | …… |
K/(mol·L-1)2 | 4×106 | 8×107 | K1 | …… |
请完成下列问题:
①判断该反应的ΔH _______0(填“>”或“<”)
②在一定条件下,能判断该反应一定达化学平衡状态的是________ (填序号)。
A. 3v(B)(正)=2v(C)(逆) B.容器内压强保持不变
C.A和B的转化率相等 D.混合气体的密度保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】下列可以大量共存的离子组是( )
A. 无色透明溶液中:NH4+、Cu2+、Cl﹣、NO3﹣
B. 碱性溶液中:K+、Na+、SO42﹣、Cl﹣
C. 酸性溶液中:K+、Na+、HCO3﹣、Ca2+
D. 酸性溶液中:Na+、Fe2+、SO42﹣、ClO﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示。
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
资料显示,反应分两步进行:
①2Fe3++ H2O2 ![]() 2Fe2++O2↑+2H+
2Fe2++O2↑+2H+
② H2O2 + 2Fe2++2H+ ![]() 2H2O+2Fe3+
2H2O+2Fe3+
反应过程中能量变化如右图所示。下列说法不正确的是
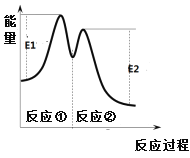
A. 0~6 min的平均反应速率:v(H2O2) = 3.33×10-2 mol·L-1·min-1
B. Fe3+的作用是加快过氧化氢的分解速率
C. 反应①是吸热反应、反应②是放热反应
D. 反应2H2O2(aq)![]() 2H2O(l) + O2(g)的△H =E1-E2 < 0
2H2O(l) + O2(g)的△H =E1-E2 < 0
查看答案和解析>>
科目: 来源: 题型:
【题目】天然气、煤炭气(CO、H2)的研究在世界上相当普遍。其中天然气和二氧化碳可合成二甲醚,二甲醚与水蒸气制氢气作为燃料电池的氢能源,比其他制氢技术更有优势.主要反应为:
①CH3OCH3(g)+H2O(g)2CH3OH(g);△H=37kJmol-1
②CH3OH(g)+H2O(g)3H2(g)+CO2(g);△H=49kJmol-1
③CO2(g)+H2(g)CO(g)+H2O(g);△H=41.3kJmol-1
其中反应③是主要的副反应,产生的CO对燃料电池Pt电极有不利影响.
请回答下列问题:
(1)二甲醚可以通过天然气和CO2合成制得,该反应的化学方程式为______________.
(2)CH3OCH3(g)与水蒸气制氢气的热化学方程式为______________.
(3)下列采取的措施和解释正确的是______________(填字母).
A.反应过程在低温进行,可减少CO的产生
B.增加进水量,有利于二甲醚的转化,并减少CO的产生
C.选择在高温具有较高活性的催化剂,有助于提高反应②CH3OH的转化率
D.体系压强升高,虽然对制取氢气不利,但能减少CO的产生
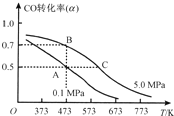
(4)煤炭气在一定条件下可合成燃料电池的另一种重要原料甲醇,反应的化学方程式为CO(g)+2H2(g)CH3OH(g);△H<0.现将10molCO与20molH2置于密闭容器中,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度、压强的关系如图所示.
①自反应开始到达平衡状态所需的时间tA________tB(填“大于”“小于”或“等于”).
②A、C两点的平衡常数KA____KC(填“大于”“小于”或“等于”).
查看答案和解析>>
科目: 来源: 题型:
【题目】利用可再生能源代替石油和煤已经成为未来发展的趋势。甲醇作为重要的可再生能源具有广泛的开发和应用前景。工业上常利用反应CO(g)+2H2(g)![]() CH3OH(g)△H<0来合成甲醇.
CH3OH(g)△H<0来合成甲醇.
(1)经研究发现在230℃~270℃时合成最为有利.为探寻合成气最合适的起始组成比,分别在230℃、250℃和270℃时进行实验,实验结果如下图。230℃的实验结果所对应的曲线是______(填字母);从提高CO转化率的角度等综合分析,该温度下工业生产适宜采用的合成气组成n(H2):n(CO)的比值范围是______(填字母).

A.1~1.5B.2.5~3C.3.5~4.5
(2)制甲醇所需要的氢气,可通过下列反应制取:H2O(g)+CO(g)![]() H2(g)+CO2(g)△H<0,某温度下该反应的平衡常数K=1.回答下列问题:
H2(g)+CO2(g)△H<0,某温度下该反应的平衡常数K=1.回答下列问题:
①该温度下,若起始时c(CO)=2mol/L,c(H2O)=3mol/L,反应进行一段时间后,测得CO的浓度为1mol/L,则此时该反应v(正)______v(逆)(填“>”、“<”或“=”).
②若降低温度,该反应的K值将______(填“增大”、“减小”或“不变”).
(3)甲醇是一种化工原料,工业上合成甲醇的反应:CO(g)+2H2(g)![]() CH3OH(g)△H=-90.8kJ/mol.
CH3OH(g)△H=-90.8kJ/mol.
若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCO、4molH2 |
CH3OH的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
①容器内压强P:P甲、P乙与P丙的关系是______(用“>”、“<”或“=”表示);
②变化的热量数值Q中,Q1与Q2的和是______(填具体数值).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com