
科目: 来源: 题型:
【题目】某无色溶液中含有Mg2+、Al3+、Fe3+、Cu2+、NH4+、Na+中的一种或几种,取100mL该溶液,向其中不断滴加NaOH溶液,产生的沉淀随着NaOH体积变化的关系如图所示, 则下列叙述不正确的是
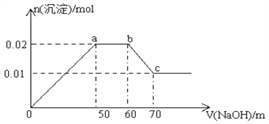
A. 该溶液中一定不含Fe3+、Cu2+
B. 该溶液中一定含有Mg2+、Al3+、NH4+,且三者物质的量浓度之比为1∶1∶1
C. 所加NaOH溶液物质的量浓度为1mol/L
D. a点到b点,没有发生化学反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒温恒容容器中,不能说明反应:C(s) +CO2(g)![]() 2CO(g)已达到平衡状态的是
2CO(g)已达到平衡状态的是
A. 每消耗1 mol CO2的同时生成2 mol CO
B. 混合气体的平均相对分子质量不再改变
C. 容器中气体的压强不再改变
D. 容器中气体的密度不再改变
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气)。下列说法正确的是
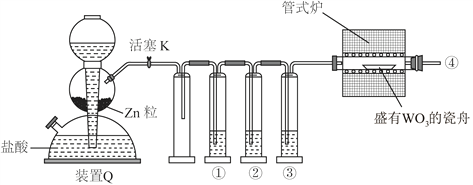
A. ①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
B. 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C. 结束反应时,先关闭活塞K,再停止加热
D. 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:
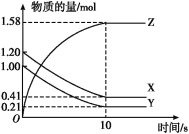
(1)从反应开始到10 s时,用Z表示的反应速率为 ,X的物质的量浓度减少了 ,Y的转化率为 。
(2)该反应的化学方程式为
(3)10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示:
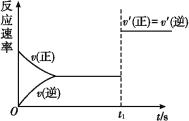
则下列说法符合该图像的是 。
A.t1时刻,增大了X的浓度 B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积 D.t1时刻,使用了催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】含碘食盐中的碘是以碘酸钾(KIO3)形式存在的。已知在酸性溶液中IO3-和I-发生下列反应IO3-+5I-+6H+=3I2+3H2O。现有下列物质①稀硫酸;②pH试纸;③淀粉碘化钾溶液;④淀粉溶液。利用上述反应,可用来检验含碘食盐中含有IO3-的是( )
A、②④ B、①③ C、②③ D、①④
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的最初生成物是
A.HCl和HIO B.HI和HClO C.HClO3和HIO D.HClO和HIO
查看答案和解析>>
科目: 来源: 题型:
【题目】A.【物质结构与性质】
甲基呋喃与氨在高温下反应得到甲基吡咯:

![]()
(1)Zn的基态原子核外电子排布式为______________。
(2)配合物[Zn(NH3)3(H2O)]2+中,与Zn2+形成配位键的原子是_____________(填元素符号)。
(3)1 mol甲基呋喃分子中含有σ键的数目为_______________mol。
(4)甲基吡咯分子中碳原子轨道的杂化轨道类型是____________。与NH3分子互为等电子体的阳离子为_____________。
(5)甲基吡咯的熔沸点高于甲基呋喃的原因是____________。
(6)锌的某种化合物晶胞结构如图所示,则构成该化合物的两种粒子个数比为____________

B.【实验化学】
硫酰氯(SO2Cl2)可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。某化学学习小组拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =97.3 kJ·mol1,实验装置如图所示(部分夹持装置未画出)。
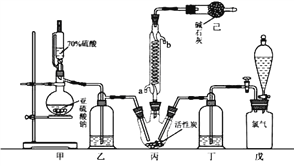
已知:硫酰氯通常条件下为无色液体,熔点54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙的冷凝管中冷凝水的入口是_____________(填“a”或“b”),装置己的作用是____________;如何控制两种反应物体积相等:______________。
(2)装置戊上方分液漏斗中最好选用下列试剂:_____________(选填字母)。
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 molL1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫发生反应的化学方程式是_____________。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H![]() SO2Cl2 + H2SO4,分离两种产物的方法是____________(选填字母)。
SO2Cl2 + H2SO4,分离两种产物的方法是____________(选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
查看答案和解析>>
科目: 来源: 题型:
【题目】从废电池外壳中回收锌(锌皮中常有少量铁、外表沾有NH4Cl、ZnCl2、MnO2等杂 质),制取ZnSO4·7H2O可以采取如下工艺流程:
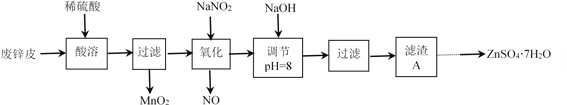
已知:①Zn(OH)2和Al(OH)3化学性质相似;②金属氢氧化物沉淀的pH:
氢氧化物 | 开始沉淀的pH | 完全沉淀的pH |
Zn(OH)2 | 5.7 | 8.0 |
Fe(OH)3 | 2.7 | 3.7 |
请回答下列问题:
(1) “酸溶”时,为了提高酸溶速率,可采取的的措施有:______________(任答一点)。
(2)“氧化”时,酸性滤液中加入NaNO2反应的离子方程式为______________。
(3) “氧化”时,为了减少污染,工业上常用H2O2替代NaNO2。
①若参加反应的NaNO2为0.2 mol,对应则至少需要加入10%H2O2溶液_______________mL(密度近似为1g·cm-3)。
②该过程中加入的H2O2需多于理论值,原因除了提高另外反应物的转化率外,还可能是_____________。
(4) “调节pH”时,若pH>8则造成锌元素沉淀率降低,其原因可能是________________。
(5)将滤渣A溶于适量稀硫酸,调节溶液pH,过滤,将滤液蒸发浓缩,冷却结晶析出ZnSO4·7H2O晶体。则该过程中需调节溶液pH的范围为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知2X2(g)+Y2(g)![]() 2Z(g)ΔH=-a kJ·mol-1(a>0),在一个容积固定的密闭容器中加入2 mol X2和1 mol Y2,在500 ℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
2Z(g)ΔH=-a kJ·mol-1(a>0),在一个容积固定的密闭容器中加入2 mol X2和1 mol Y2,在500 ℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
(1)此反应平衡常数表达式为___________;若将温度降低到300 ℃,则反应平衡常数将________(填“增大”“减少”或“不变”)。
(2)若原容器中只加入2 mol Z,500 ℃充分反应达平衡后,吸收热量c kJ,则Z浓度________W mol·L-1(填“>”“<”或“=”),b、c间的关系为________。(用a、b、c表示)。
(3)能说明反应已达到平衡状态的是________。
a.单位时间内消耗1molY2的同时消耗了2molZ b.容器内的密度保持不变
c. v逆(X2)=2v正(Y2) d.容器内压强保持不变
e.混合气体的平均式量保持不变 f.Y2和X2的转化率相等
(4)若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2 mol X2和1 mol Y2,达到平衡后,Y2的转化率将________(填“变大”“变小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应4NH3(g)+5O2(g)4NO(g)+6H2O(g)在两升密闭容器中进行1分钟后,NH3减少了0.12mol,则平均每秒钟浓度变化正确的是( )
A.NO 0.001 molL﹣1
B.H2O 0.002 molL﹣1
C.NH3 0.002 molL﹣1
D.O2 0.0025 molL﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com