
科目: 来源: 题型:
【题目】鉴别甲烷、乙烯、乙炔三种气体可采用的方法是 ( )
A.通氢气,观察体积变化B.通入溴水中,观察溴水是否褪色
C.点燃,检验燃烧产物D.点燃,观察火焰明亮程度及产生黑烟量的多少
查看答案和解析>>
科目: 来源: 题型:
【题目】关于实验,下列说法正确的是
|
|
A.模拟工业制氨气并检验产物 | B.一段时间后,试管中固体变为红棕色 |
|
|
C.可用所示装置比较KMnO4、Cl2、S的氧化性强弱 | D.若溴水褪色则证明石蜡油分解产生乙烯 |
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 用pH试纸检测:0.1 mol·L1 Na2SO3溶液、0.1 mol·L1 NaHSO3溶液 | Na2SO3溶液的pH约为10;NaHSO3溶液的pH约为5 |
|
B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | Na2CO3溶液中存在水解平衡 |
C | 注射器中吸入NO2,封堵针尖处,将注射器体积压缩为原来的一半 | 气体颜色比起始时浅 | 加压后,NO2转变为无色的N2O4 |
D | 饱和BaSO4悬浊液中加入饱和Na2CO3溶液,振荡,然后过滤、洗涤,向所得固体中加入盐酸 | 沉淀部分溶解且有气体产生 | Ksp(BaSO4) > Ksp(BaCO3) |
查看答案和解析>>
科目: 来源: 题型:
【题目】依据下列事实或实验得出结论正确的是
选项 | 事实或实验 | 结论 |
A | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
B | 向某溶液中滴加氨水,再加入KSCN溶液,溶液呈红色 | 原溶液中一定含有Fe2+ |
C | 汽车尾气净化反应2NO(g) + 2CO(g) | 该反应在常温下不能自发进行 |
D | 向NaBr溶液中滴入少量氯水和CCl4,振荡、静置,溶液下层呈橙红色 | Br还原性强于Cl |
查看答案和解析>>
科目: 来源: 题型:
【题目】现用密度为1.2g/mL、质量分数为36.5%的浓盐酸来配制90mL 0.8mol/L的稀盐酸.可供选择的仪器有:①玻璃棒 ②托盘天平 ③50mL烧杯 ④药匙 ⑤胶头滴管 ⑥量筒.
请回答下列问题:
(1)上述仪器中,在配制稀盐酸时需要使用的有(填序号),还缺少的仪器是(填仪器名称).
(2)计算:所需浓盐酸的物质的量浓度为 , 量取浓盐酸的体积为mL.量取浓盐酸时应选用量筒的规格为
①10mL ②50mL ③100mL
(3)将所配制的稀盐酸进行测定,发现浓度大于0.8mol/L.请你分析配制过程中可能引起浓度偏高的原因(答出两点)、 .
查看答案和解析>>
科目: 来源: 题型:
【题目】等物质的量浓度的下列物质的溶液,其pH由小到大的顺序排列正确的是( ):
①CH3COONa ②NaOH ③NaNO3④HCl⑤Al2(SO4)3.
A. ①②③④⑤ B. ⑤④③②① C. ④⑤③①② D. ④⑤②①③
查看答案和解析>>
科目: 来源: 题型:
【题目】把少量的MnO2粉末加入50mL过氧化氢的溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
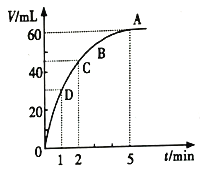
回答下列问题:
(1)实验时放出气体的总体积为________。
(2)放出一半气体所需要的时间为________。
(3)反应放出![]() 气体所需要的时间为________。
气体所需要的时间为________。
(4)A、B、C、D各点反应速率的快慢顺序为________。
(5)反应速率变化的原因________。
(6)可以代替MnO2粉末的物质有(答出1种即可) ________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一容积为2L的密团容器内加入0.2molN2和0.6molH2,在一定条件下发生如下反应: ![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g)![]() NH3(g)
NH3(g)
①该反应的平衡常数的表达式是:____________。
②反应中氨气的浓度的变化情况如图所示,计算从反应开始到平衡时,平均反应速率v(H2)=________。

③判断该反应达到平衡状态的标志是_________。
a.N2和NH3浓度相等 b.NH3百分含量保持不变
c.容器中气体的压强保持不变 d.NH3的生成速率与H2的消耗速率相等
e.容器中混合气体的密度保持不变
④反应达平衡后,第5分钟末,保持其它条件不变,仅改变反应温度,则NH3的物质的量浓度不可能为______。
a.0.2mol/L b.0.12mol/L c.0.10mol/L d.0.08mol/L
⑤在第5分钟末,将容器体积缩小一半后,若在第8分钟末达到新平衡(此时NH3浓度约为0.25mol/L),请在上图中画出从第5分钟末开始,再达到新平衡时NH3浓度变化曲线。______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com