
科目: 来源: 题型:
【题目】类比是重要的化学学科方法,类比pH的定义可定义pOH 和pKW。在水的电离平衡中,c(H+)和c(OH-)的关系如图所示,则下列说法不正确的是:
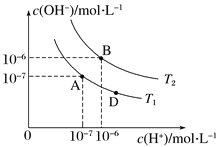
A. 图中温度T2>25 ℃
B. 位于AB直线上任意点的溶液均有c(H+)= ![]()
C. 位于AB直线上任意点的溶液均有pH=pOH =![]()
D. 图中D点处的溶液显碱性
查看答案和解析>>
科目: 来源: 题型:
【题目】高分子化合物G是作为锂电池中Li十迁移的介质,合成G的流程如下:
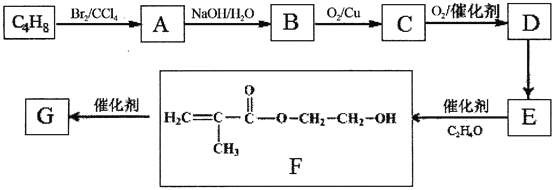
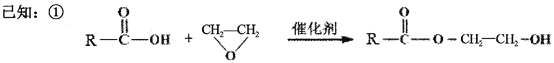
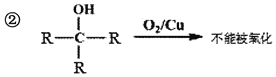
(1)B的含氧官能团名称是_____________________________________。
(2)A—B的反应类型是_____________________________________。
(3)C的结构简式是_____________________________________。
(4)D→E反应方程式是_____________________________________。
(5)G的结构简式是_____________________________________。
(6)D的一种同分异构体,能发生分子内酯化反应生成五元环状化合物,该同分异构体的结构简式是_____________________________________。
(7)已知: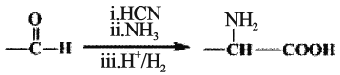
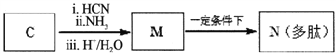
M—N的化学方程式是___________________________。
(8)下列说法正确的是_______________(填字母)。
a.E有顺反异构体
b.C能发生加成、消去反应
c.M既能与酸反应,又能与碱反应
d.苯酚与C反应能形成高分子化合物
e.含有—OH和—COOH的D的同分异构体有2种
查看答案和解析>>
科目: 来源: 题型:
【题目】关于生物体内有机化合物所含元素的叙述,错误的是 ( )
A. 叶绿素含有镁元素 B. 血红蛋白含有铁元素
C. 脱氧核糖含有磷元素 D. 胰岛素含有氮元素
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学与生产、生活的说法中,不正确的是 ( )
A.陶瓷、水泥和玻璃都属于硅酸盐产品
B.低温下甲醇与水蒸气催化制氢,该反应属于氧化还原反应
C.铝合金的大量使用归功于人们能使用焦炭从氧化铝中获得铝
D.屠呦呦用乙醚从青蒿中提取出对治疗疟疾有特效的青蒿素,该过程包括萃取操作
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO![]() 2CO2+N2 △H <0。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2 △H <0。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:

请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①前2s内的平均反应速率v (N2) = ___________。
②假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是______。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(2)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH=_____kJ·mol-1。
SO3(g)+NO(g)的ΔH=_____kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=_________。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH_______0(填“>”或“ <”)。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH_______0(填“>”或“ <”)。

查看答案和解析>>
科目: 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)在一定条件下将CO2和H2转化为甲醇蒸气和水蒸气的相关反应有:
CO2(g)+H2(g)![]() CO(g)+H2O(g) △H1=+41kJ/mol
CO(g)+H2O(g) △H1=+41kJ/mol
CO(g)+2 H2(g)![]() CH3OH(g) △H2=-90kJ/mol
CH3OH(g) △H2=-90kJ/mol
则由CO2和H2转化为甲醇蒸气和水蒸气的热化学方程式为____________________。
(2)在一定温度下,向2L固定容积的密闭容器中通入2molCO2、3molH2,发生反应CO2(g)+3H(g)2![]() CH3OH(g)+H2O(g) △H3<0.测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H3<0.测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
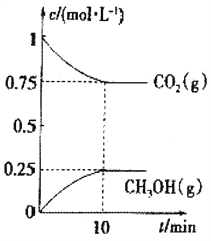
①能说明该反应已达平衡状态的是______________。
A.单位时间内有n molH—H键断裂,同时又n mol O—H键生成
B.混合气体的密度不随时间变化
C.体系中n(CO2)/n(H2)=1∶1,且保持不变
D.CO2的体积分数在混合气体中保持不变
②下列措施能使n(CH3OH)/n(CO2)增大的是__________。
A.升高温度
B.恒温恒容下,再充入2molCO2、3molH2
C.使用高效催化剂
D.恒温恒容充入He(g)
③计算该温度下此反应的平衡常数K=__________(L/mol)2(保留3位有效数字);若使K的值变为1,则应采取的措施是___________。
A.增大压强 B.恒压加入一定量H2
C.升高温度 D.降低温度
(3)捕捉CO2可以利用Na2CO3溶液。用100mL 0.1mol/LNa2CO3溶液完全捕捉224mL(己换算为标准状况,溶液体积变化忽略不计)CO2气体,所得溶液显_________性(填酸,碱,中):且c(HCO3-)+c(CO32-)+c(H2CO3)=__________mol/L(填数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氰化钠(NaCN)是一种重要的化工原料,用于电镀、冶金和有机合成医药,农药及金属处理等方面。已知:氰化钠为白色结晶颗粒或粉末,易潮解,有微弱的苦杏仁气味,剧毒。熔点563.7℃,沸点1496℃。易溶于水,易水解生成氰化氢,水溶液呈强碱性。
(1)氰化钠中碳元素的化合价+2价,N元素显-3价,则非金属性N__________C(填<,=或 >),用离子方程式表示NaCN溶液呈强碱性的原因:____________________。
(2)己知:
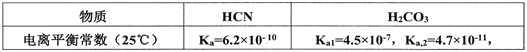
则向NaCN溶液通入少量CO2反应的离子方程式:____________________
(3)用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法错误的是________________。
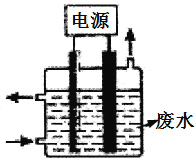
A.除去CN-的反应:2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O
B.用石墨作阳极,铁作阴极
C.阴极的电极反应式为:2H2O+2e-=H2↑+2OH-
D.阳极的电极反应式为:Cl-+2OH--2e-=ClO-+H2O
(4)氰化钠可用双氧水进行消毒处理。
用双氧水处理氰化钠产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式____________________;
(5)化合物(CN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,试写出(CN)2与NaOH溶液反应的化学方程式:____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.同温同压下甲烷和氧气的密度之比为2:1
B.1 g甲烷和1 g氧气的原子数之比为5:1
C.等物质的量的甲烷和氧气的质量之比为2:1
D.在标准状况下等质量的甲烷和氧气的体积之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com