
科目: 来源: 题型:
【题目】次氯酸钠(NaClO)是漂白液的主要成分,次氯酸钠溶液可用于消毒、杀菌及水处理。一种生产次氯酸钠的工艺如图所示。
-
(1)Cl 元素位于元素周期表第______周期___族。
(2)写出NaOH的电子式:__________。
(3)写出反应②的化学方程式:_______________。该反应中每生成1mol NaClO时,转移______mol 电子。
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是_____________________(用离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。
(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应:COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H=-34kJ/mol
H2S(g)+CO2(g) △H=-34kJ/mol
氢解反应:COS(g)+H2(g) ![]() H2S(g)+CO(g) △H=+7kJ/mol。
H2S(g)+CO(g) △H=+7kJ/mol。
已知:2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol。
写出表示CO燃烧热的热化学方程式:______________。
(2)氢解反应达到平衡后,保持体系的温度和总压强不变,通入适量的He,正反应速率____(填“增大”“减小”或“不变”,下同),COS的转化率_______。
(3)某温度下,向体积为2L的恒容密闭容器中通入2molCOS(g)和4molH2O(g),发生水解反应,5min后反应达到平衡,测得COS(g)的转化率为75%。
回答下列问题:
①反应从起始至5min内,v(H2S)=_______mol·L-1·min-1。
②该温度下,上述水解反应的平衡常数K=____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外研究性学习小组拟用粗盐(含有少量杂质包括:泥沙、CaCl2、MgCl2、Na2SO4)经提纯后,配制0.4mol/L 450mL NaCl溶液.他们设计并实施了如下实验,请根据已学过的知识回答下列问题:
(1)取一定量的粗盐置于烧杯中加水溶解,所加的水量应为: . (填选项)
A.多加水配成较稀的溶液
B.加入适量的水至能溶解的固体溶解即止
(2)将(1)中配制的粗盐悬浊液过滤后取滤液加入过量的除杂试剂,如果除杂试剂可从下列六种溶液中选择 ①Na2CO3溶液 ②KOH溶液 ③AgNO3溶液 ④NaOH溶液 ⑤NaHCO3溶液 ⑥BaCl2溶液,则正确的试剂和加入的顺序应为 . (填选项,多选、少选、错选都不得分)
A.①②③B.②⑥⑤C.④⑥①D.①④⑥E.⑥①④F.⑥②⑤
将所得的悬浊液经过滤后取滤液加入足量的盐酸,充分反应后对混合溶液进行蒸发、过滤、洗涤、干燥操作,得到纯净的NaCl固体,请描述在蒸发操作过程中玻璃棒的作用是 .
(3)利用(2)中所得的NaCl固体继续配制所需溶液.在托盘天平上称量g NaCl固体.配制过程中需要使用的玻璃仪器有:烧杯、玻璃棒、和 .
(4)配制结束后同学们对实验中出现的某些错误操作,对最终配制的溶液浓度的影响进行了分析,则下列错误操作会导致最终配制溶液中NaCl的浓度相比0.4mol/L的偏差是:(填“偏大”、“偏小”、“无影响”)
①在上述(2)步中没有使用盐酸处理滤液,结果会 ,
②定容时俯视凹液面,结果会
③上下颠倒摇匀后液面低于刻度线,未及时加水至刻度线,结果会
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外研究性学习小组拟用粗盐(含有少量杂质包括:泥沙、CaCl2、MgCl2、Na2SO4)经提纯后,配制0.4mol/L 450mL NaCl溶液.他们设计并实施了如下实验,请根据已学过的知识回答下列问题:
(1)取一定量的粗盐置于烧杯中加水溶解,所加的水量应为: . (填选项)
A.多加水配成较稀的溶液
B.加入适量的水至能溶解的固体溶解即止
(2)将(1)中配制的粗盐悬浊液过滤后取滤液加入过量的除杂试剂,如果除杂试剂可从下列六种溶液中选择 ①Na2CO3溶液 ②KOH溶液 ③AgNO3溶液 ④NaOH溶液 ⑤NaHCO3溶液 ⑥BaCl2溶液,则正确的试剂和加入的顺序应为 . (填选项,多选、少选、错选都不得分)
A.①②③B.②⑥⑤C.④⑥①D.①④⑥E.⑥①④F.⑥②⑤
将所得的悬浊液经过滤后取滤液加入足量的盐酸,充分反应后对混合溶液进行蒸发、过滤、洗涤、干燥操作,得到纯净的NaCl固体,请描述在蒸发操作过程中玻璃棒的作用是 .
(3)利用(2)中所得的NaCl固体继续配制所需溶液.在托盘天平上称量g NaCl固体.配制过程中需要使用的玻璃仪器有:烧杯、玻璃棒、和 .
(4)配制结束后同学们对实验中出现的某些错误操作,对最终配制的溶液浓度的影响进行了分析,则下列错误操作会导致最终配制溶液中NaCl的浓度相比0.4mol/L的偏差是:(填“偏大”、“偏小”、“无影响”)
①在上述(2)步中没有使用盐酸处理滤液,结果会 ,
②定容时俯视凹液面,结果会
③上下颠倒摇匀后液面低于刻度线,未及时加水至刻度线,结果会
查看答案和解析>>
科目: 来源: 题型:
【题目】“朴雪”乳酸亚铁口服液可以有效地治疗人类缺铁性贫血症,这是因为其中的 Fe2+进入人体后能
A. 调节血液的酸碱平衡
B. 调节血液的渗透压
C. 参与红细胞血红蛋白的形成
D. 促进更多红细胞的产生
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于元素的说法正确的是( )
A.随着人工合成的同位素种类不断增加,许多元素的相对原子质量也会随之变化
B.第ⅠA族都是金属元素
C.短周期主族元素的族序数一定等于原子的最外层电子数
D.周期表中非金属元素均位于过渡元素右侧
查看答案和解析>>
科目: 来源: 题型:
【题目】微量元素是指其质量不到人体体重万分之一的元素。微量元素对体内正常代谢和健康起着重要作用。下列元素不属于微量元素的是
A. Fe B. I C. H D. F
查看答案和解析>>
科目: 来源: 题型:
【题目】在实验室中严禁打闹,某几个同学在做实验中打闹而同时把盛有浓盐酸和盛固体KClO3的试剂瓶打破,使其在地上混合立即产生大量黄绿色气体,发生反应的化学方程式为:
KClO3+6HCl(浓) ![]() KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O
(1)该反应中的氧化剂是 .
(2)在化学方程式上标出电子转移的方向和数目 .
(3)如反应中转移了0.50mol电子,则产生的气体在标准状况下体积为L.
(4)在清除碎片时某同学用湿毛巾捂住鼻子防止中毒,有以下四种溶液可浸湿毛巾,它们分别是:①NaOH溶液 ②NaCl溶液 ③KBr溶液 ④NaHCO3溶液.正确选择是(填试剂号数)
查看答案和解析>>
科目: 来源: 题型:
【题目】用无机矿物资源生产部分材料,其产品流程示意图如下:
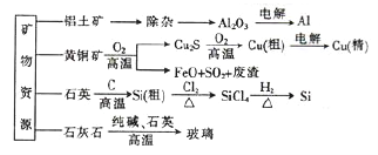
下列有关说法不正确的是
A. 制取粗硅时生成的气体产物为CO2
B. 生产铝、铜、高纯硅过程中涉及氧化还原反应
C. 黄铜矿冶炼铜时产生的副产物中,SO2可用于生产硫酸,FeO可用作冶炼铁的原料
D. 玻璃的生产工业属于硅酸盐工业,玻璃与水泥一样,主要成分都是硅酸盐
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生活、生产、社会可持续发展密切相关。下列说法错误的是
A.利用硫酸钡不溶于水也不溶于酸的性质,使其作X射线透视肠胃的造影剂
B.有些肾病患者要定期进行血透,血透原理是利用渗析的方法净化血液
C.禁止使用四乙基铅作汽油抗爆震剂,可减少环境中的铅污染
D.蒸馏“地沟油”可以获得汽油
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com