
科目: 来源: 题型:
【题目】工业上,以钛铁矿为原料制备二氧化钛的工艺流程如下图所示。钛铁矿主要成分为钛酸亚铁(FeTiO3,难溶于水),其中一部分铁元素在风化过程中会转化为+3价。

已知:TiOSO4遇水会水解。
(1)步骤①中,钛酸亚铁与硫酸反应的离子方程式为__________________。
(2)步骤③中,实现混合物的分离是利用物质的___________(填字母序号)。
a. 熔沸点差异 b. 溶解性差异 c. 氧化性、还原性差异
(3)步骤④的操作是_______________(填操作名称)。
(4)步骤④中将TiO2+转化为H2TiO3的原理TiO2++2H2O ![]() H2TiO3+ 2H+,该反应的△H_______0(填>或<);加水稀释,平衡_________(填“正向”、“逆向”或“不”)移动。
H2TiO3+ 2H+,该反应的△H_______0(填>或<);加水稀释,平衡_________(填“正向”、“逆向”或“不”)移动。
(5)可以利用生产过程中的废液与软锰矿(主要成分为MnO2)反应生产硫酸锰(MnSO4,易溶于水),该反应的离子方程式为__________________________。
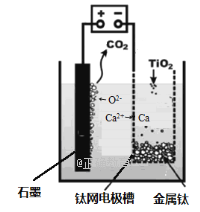
(6)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。在制备金属钛前后,CaO的总量不变,其原因是(请用化学方程式解释)______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列物质中,属于强电解质的是(填序号,下同)__________,属于弱电解质的是________,属于非电解质_____________;
①氨气 ②氨水 ③盐酸 ④醋酸 ⑤硫酸钡 ⑥氯化银 ⑦氯化钠 ⑧二氧化碳 ⑨醋酸铵 ⑩氢气
(2)常温下,取0.2 mol/L HCl溶液与0.2mol/L MOH溶液等体积混合,测得混合后溶液的pH=5。写出MOH的电离方程式:__________________。
(3)甲、乙两瓶氨水的浓度分别为1 molL-1、0.1 molL-1,则c(OH﹣)甲 :c(OH﹣)乙_________10(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】镭是元素周期表中第七周期第IIA族元素,关于其叙述不正确的是( )
A. 镭的金属性比钙弱B. 单质能与水反应生成H2
C. 在化合物中呈+2价D. 碳酸镭难溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究浓硫酸的性质,设计了如下图所示的装置进行实验. 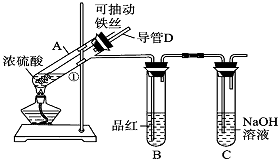
(1)用“可抽动的铁丝”代替“直接投入铁片”的优点是 .
(2)说明SO2气体产生的实验现象是;装置C的作用是 .
(3)反应一段时间后,他们对试管A中溶液的金属离子进行探究,请完成相关试题:
①提出假设:假设1:只含有Fe3+;
假设2:只含有Fe2+;
假设3:既有Fe2+ , 又有Fe3+ .
②请设计实验方案验证假设3.
限选试剂:稀硫酸、KMnO4溶液、KSCN溶液、NaOH溶液、H2O2溶液.
实验步骤 | 预期现象 |
步骤一:用胶头滴管取出A试管中的溶液,用水稀释后,并分装在试管Ⅰ、Ⅱ中备用 | |
步骤二:检验Fe3+ , 往试管Ⅰ中, | |
步骤三:检验Fe2+ , 往试管Ⅱ中, |
(4)已知C+2H2SO4(浓) ![]() 2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的性.
2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的性.
A.脱水性 B.强氧化性 C.吸水性
若要验证反应产物中同时混有SO2气体和CO2气体,可选择以下试剂进行实验:
①NaOH溶液②品红溶液③溴水④Ca(OH)2溶液,选择合适试剂并安排合理的顺序为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】氮氧化物进入大气后,可能会形成硝酸型酸雨,因此必须对含有氮氧化物的废气进行处理.
(1)用NaOH可以吸收废气中的氮氧化物,反应的化学方程式如下:
2NO2+2NaOH═NaNO2+NaNO3+H2O 反应中,还原剂是 ,
NO2+NO+2NaOH═2NaNO2+H2O 反应中,氧化产物和还原产物之比为 .
(2)NO2和Br2蒸汽都是红棕色气体,下列可以用来鉴别这两种气体的试剂是 .
A.用氢氧化钠溶液
B.淀粉碘化钾溶液
C.用硝酸银溶液
D.用蒸馏水
(3)汽车尾气中含有一氧化氮和一氧化碳,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成两种对大气无污染的气体,该反应的化学方程式为 .
(4)氨气也可用来处理氮氧化物,例如:氨气与二氧化氮反应生成氮气和水,写出该反应的化学方程式: , 若某工厂排出的废气中二氧化氮含量为0.5%(体积分数),处理1000m3(标准状况)这种废气,需要千克氨气.(结果保留两位小数)
查看答案和解析>>
科目: 来源: 题型:
【题目】鉴别二甲醚和乙醇可采用化学方法或物理方法,下列方法不能对二者进行鉴别的是( )
A.利用金属钠或金属钾法
B.利用红外光谱法
C.利用质谱法
D.利用核磁共振氢谱法
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F2+离子核外各层电子均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为____。(用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是____________________。
(3)E的最高价氧化物分子的空间构型是__________,是____分子(填“极性”“非极性”)。
(4)F原子的核外电子排布式是________________。
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子),其化学式为_________。(a)中E原子的配位数为____。若在(b)的结构中取出一个平行六面体作为晶胞,则平均一个晶胞中含有____个F原子。结构(a)与(b)中晶胞的原子空间利用率相比,(a)____(b)(填“>”“<”或“=”)。
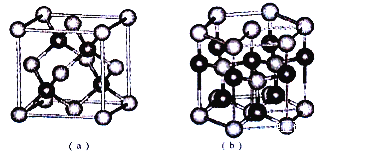
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质被略去.常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质,G、J的焰色均为黄色.反应①为炼铁高炉中的重要反应;反应②可用于焊接铁轨.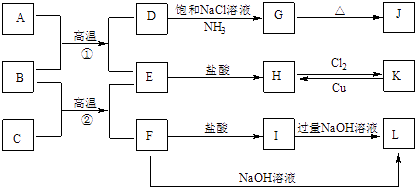
请回答下列问题:
(1)B的化学式为 , J的化学式为
(2)工业上将氯气通入石灰乳中制取漂白粉,该反应的化学反应方程式为
(3)D→G是侯氏制碱法的主要反应,该反应的化学方程式为 .
(4)K→H是制作印刷电路板的重要反应,该反应的离子方程式为 .
(5)F→L是铝土矿提纯中的重要反应,该反应的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com