
科目: 来源: 题型:
【题目】下列有关混合物的分离方法中,正确的是( )
A.从食盐溶液中获得食盐晶体采用蒸发的方法
B.除去酒精中含有的少量水采用萃取的方法
C.将碘晶体中含有的少量沙子除去采用蒸馏的方法
D.从碘水中获得碘晶体采用过滤的方法
查看答案和解析>>
科目: 来源: 题型:
【题目】三氧化二铬可用作搪瓷、陶瓷、人造革、建筑材料的着色剂。由高碳铬铁合金(含Cr、Fe及C)制备三氧化二铬的工艺流程如下:
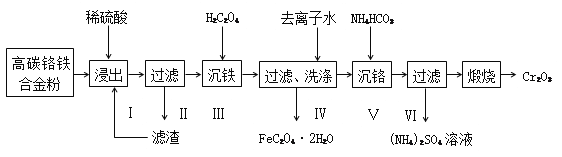
已知:Cr(OH)3是两性氢氧化物,草酸亚铁为微溶物。
回答下列问题:
(1)步骤Ⅰ浸取时,为提高浸取速率,除将高碳铬铁合金制成粉末外,还可采取的措施是__________________________(写一点);浸取铬时反应的离子方程式为_______________。
(2)步骤Ⅱ滤渣返回再次浸取的目的是_____________________________________________。
(3)步骤Ⅲ除铁时,溶液的pH对铁的去除率影响如图1所示:

图1 图2
pH小于2.3时,铁去除率低,其原因是_______________________________________。
(4)步骤Ⅳ能说明沉淀已洗涤干净的操作是________________________________________。
(5)步骤Ⅴ沉铬时,生成Cr(OH)3的化学方程式为_____________________________;沉铬时,溶液pH与铬的回收率关系如图2所示,当pH>8.5时,pH越大,铬的回收率越低,其可能原因是____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元索W、X、Y、Z的原子序数依次增加。Z单质是常见的黄绿色气体,u是Y的最高价氧化物且具有两性,v是X的最高价氧化物对应的水化物。常温下,0.01mol·L-1 v溶液的pH为12,0.01 mol·L-1 r溶液的pH为2,上述物质的转化关系如图所示。下列说法正确的是
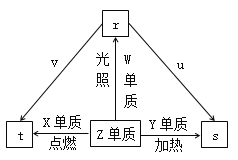
A. 单质沸点:W>Z
B. 原子半径:X>Z>W
C. Y、Z形成的化合物中化学键的类型是离子键
D. X的简单离子比Y的简单离子氧化性强
查看答案和解析>>
科目: 来源: 题型:
【题目】铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4[UO2(CO3)3]等。回答下列问题:
(1)UF4用Mg或Ca还原可得金属铀。金属铀的一种堆积方式为体心立方堆积,该堆积方式的空间利用率为__________________;基态钙原子核外电子排布式为_________________;熔点:MgO(2852℃)高于CaO(2614℃),其原因是_____________________________。
(2)![]() 。NH4HF2中所含作用力有____________(填字母)。
。NH4HF2中所含作用力有____________(填字母)。
a. 氢键 b. 配位键 c. 共价键 d. 离子键 e. 金属键
(3)已知: ![]() .
.
①NH4+ 的空间构型为___________,与NH4+ 互为等电子体的分子或离子有_____(写两种)
②CO32- 中碳原子杂化轨道类型为______________________。
③分解产物中属于非极性分子的是_____________________(填字母)。
a. NH3 b. CO2 c. N2 d. H2O
(4)UO2 的晶胞结构及晶胞参数如下图所示:
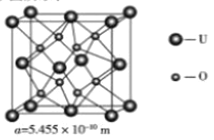
①晶胞中U的配位数为_________________。
②UO2 的密度为__________g·cm-3(列出计算式即可,用NA表示阿伏伽德罗常数的值)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在水溶液中能大量共存的离子组是
A. Al3+ H+ HCO3- Cl- B. Na+ AlO2- OH- SO42-
C. Ca2+ K+ NO3- CO32- D. H+ Fe2+ MnO4- NO3-
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)2NH3(g)
(1)若反应进行到某时刻t时,n1(N2)=13mol,n1(NH3)=6mol,计算a的值.
(2)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数)为25%.计算平衡时NH3的物质的量.
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同).n1(始):n1(平)= .
(4)原始混合气体中,a:b= .
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室有四个药品橱,已存放如下药品:
橱 | 甲橱 | 乙橱 | 丙橱 | 丁橱 |
药品 | 盐酸、硫酸 | CCl4、C2H5OH | 红磷、硫 | 铜、锌 |
实验室新购进一些活性炭,应将它存放在
A. 甲橱 B. 乙橱 C. 丙橱 D. 丁橱
查看答案和解析>>
科目: 来源: 题型:
【题目】向某晶体的水溶液中加入Fe2+的溶液后,无明显变化,当滴加几滴溴水后,混合液出现血红色。则由此得出下列的结论错误的是
A. 该晶体中一定含有SCN-
B. Fe3+的氧化性比Br2的氧化性强
C. Fe2+被Br2氧化为Fe3+
D. Fe2+与SCN-不能形成血红色的化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】在一密闭的2L容器中装有4mol SO2和2mol O2 , 在一定条件下开始反应.2min末测得容器中有1.6mol SO2 , 请计算:
(1)2min末SO3的浓度;
(2)2min内SO2的平均反应速率.
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用下图实验装置验证通过改变浓度来实现反应2Fe3++2I-=2Fe2++I2中Fe3+与Fe2+的相互转化。K闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反。下列有关说法不正确的是
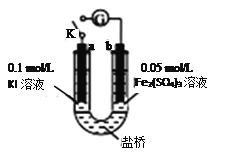
A. 指针第一次偏转时,b极反应式为Fe3++e-=Fe2+
B. 加入AgNO3后,a为正极
C. 第二次指针偏转的原因是:I-浓度减小,反应逆向进行
D. 当b极有0.001 mol Fe3+被还原时,则通过盐桥的电子数为0.001 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com