
科目: 来源: 题型:
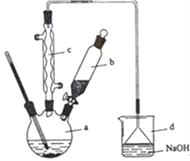
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:按下列合成步骤回答问题:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/°C | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了_____气体。继续滴加至液溴滴完。装置d的作用是________;制取溴苯的化学方程式____________________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是:______。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为_______________,要进一步提纯,下列操作中必须的是_________(填入正确选项前的字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)取反应后烧杯中的溶液2 mL加入足量的稀硝酸酸化,再滴入AgNO3溶液,有浅黄色沉淀生成___(能或不能)证明苯与液溴反生了取代反应,为什么? _______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】燃烧法是测定有机化合物分子式的一种重要方法.完全燃烧0.05mol某烃A后,将燃烧产物依次通过足量浓硫酸、碱石灰,试验结束后,称得浓硫酸增重5.4g,碱石灰增重11g.则:
(1)该烃的分子式为;属于烃.
(2)写出烃A所有可能存在的结构简式;
(3)若烃A的一氯取代产物只有一种,写出A与氯气反应(第一步)的化学方程式;
(4)下列烃中,属于A的同系物,且其一氯代物可能只有一种的是; A:C3H8 B:C2H4 C:C8H18 D:C6H14
(5)在120°C和101Kpa的条件下,某气态烃和一定质量的氧气混合点燃,完全反应后再恢复到原来的温度时,气体体积不变,则该烃可能是 .
A.CH4
B.C2H2
C.C2H4
D.C2H6 .
查看答案和解析>>
科目: 来源: 题型:
【题目】根据题意解答
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu═2FeCl2+CuCl2 , 若将此反应设计成原电池,则负极所用电极材料为 , 当线路中转移0.1mol电子时,则被腐蚀铜的质量为g,正极的电极方程式为 .
(2)已知甲醇燃料电池的工作原理如图所示. 
该电池工作时,b口通入的物质为 , 该电池正极的电极反应式为: , 工作一段时间后,当6.4g甲醇(CH3OH)完全反应生成CO2时,有mol电子发生转移.
(3)若将(3)中电池的电解质溶液换为KOH溶液,则负极的电极方程式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】制备氮化镁的装置示意图如下:

回答下列问题:
(1)检查装置气密性的方法是______________________,a的名称是_____________________。
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式___________________________________。
(3)C的作用是________________________,D的作用是________________,是否可以把C和D的位置对调并说明理由_________________________________。
(4)写出E中发生反应的化学方程式_____________________________________。
(5)请用化学方法确定是否有氮化镁生成,并检验是否含有未反应的镁,写出实验操作及现象_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:

请回答下列问题:
(1)当(NH4)2SO4,NH3·H2O的混合溶液中存在c(NH4+)=2c(SO42-)时,溶液呈___________ (填“酸”、“碱”或“中”)性。
(2)“浸取”时为了提高锌的浸出率,可采取的措施是__________________(任写一种)。
(3)“浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为____________________________。
(4)“沉锌”的离子方程式为__________________________________。
(5)“过滤III”所得滤液可循环使用,其主要成分的化学式是__________________。
(6)己知:HCN的电离常数Ka=4.9×10 -10, H2S 的电离常数Ka1=1.3×10 -7,Ka2=7.0×10 -15,向NaCN 溶液中通入少量的H2S 气体,反应的离子方程式为______________________________________。在废水处理领域中常用H2S 将Mn2+转化为MnS 除去,向含有0.020 molL-1Mn2+废水中通入一定量的H2S 气体,调节溶液的pH=a,当HS-浓度为1.0×10 -4molL-1时,Mn2+开始沉淀,则a=____________。[已知: Ksp(MnS)=1.4×10 -15]
查看答案和解析>>
科目: 来源: 题型:
【题目】研究氮及其化合物的转化在实际工业生产、生活中具有重要的意义。
(1)已知工业上合成氨N2(g)+3H2(g)![]() 2NH3(g)的能量变化如图所示,在一定温度下,向2 L的恒容密闭容器中投入2.2 mol N2和2.6 mol H2,经10 min达到平衡,测得以氢气表示的平均速率为0.03mol·L-1·min-1
2NH3(g)的能量变化如图所示,在一定温度下,向2 L的恒容密闭容器中投入2.2 mol N2和2.6 mol H2,经10 min达到平衡,测得以氢气表示的平均速率为0.03mol·L-1·min-1
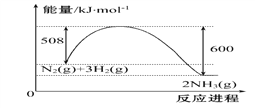
①该反应的热效应△H=______________
②反应达到平衡后放出的热量为__________kJ,此时N2的转化率为___________;在该温度下,反应的平衡常数K=__________
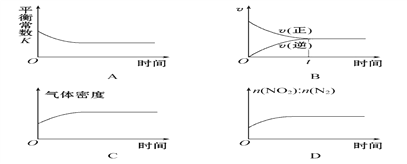
(2)利用炽热的活性炭可以处理NO2,反应原理为2C(s)+2NO2(g)![]() 2CO2(g)+N2(g),一定温度下,将一定量的活性炭和NO2加入一恒容密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________(填序号)。
2CO2(g)+N2(g),一定温度下,将一定量的活性炭和NO2加入一恒容密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________(填序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是金属镁和卤素反应的能量变化图(反应物和生成物均为298 K时的稳定状态)。下列选项中不正确的是( )
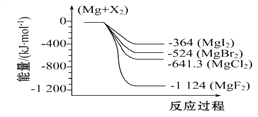
A. Mg与F2反应的ΔS<0 B. MgF2(s)+Br2(l)MgBr2(s)+F2(g)ΔH=+600 kJ·mol-1
C. MgBr2与Cl2反应的ΔH<0 D. 化合物的热稳定顺序:MgI2>MgBr2>MgCl2>MgF2
查看答案和解析>>
科目: 来源: 题型:
【题目】现有部分短周期元素的性质、应用或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | M层电子数是K层电子数的3倍 |
X | 一种同位素可测定文物年代 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(1)元素X可测定文物年代的同位素符号是 .
(2)元素Z在周期表中的位置为 . Y单质的结构式为 .
(3)元素Y与氢元素形成一种离子YH4+ , 实验室检验溶液中含有这种离子方法是:(仅用离子反应方程式表示).
(4)元素Z与元素T相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是 . a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.Z的最高价氧化物对应水化物的酸性比T的最高价氧化物对应水化物的酸性强.
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,将0.6 mol A和0.5 mol B充入0.4 L密闭容器中发生2A(g)+B(g)![]() mD(g)+E(g),经过5 min后达到化学平衡,此时测得D为0.2 mol。又知5 min内用E表示的平均反应速率为0.1 mol·L-1·min-1,下列结论正确的是( )
mD(g)+E(g),经过5 min后达到化学平衡,此时测得D为0.2 mol。又知5 min内用E表示的平均反应速率为0.1 mol·L-1·min-1,下列结论正确的是( )
A. A、B均转化了20% B. m值为2
C. 该温度下,反应的平衡常数K为1.33L·mol-1 D. 平衡时混合物总物质的量为1 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下图判断,下列说法正确的是( )
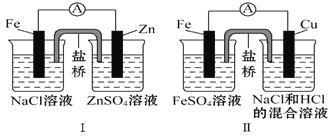
A. 装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-Fe2+
B. 装置Ⅰ和装置Ⅱ中正极反应均是O2+2H2O+4e-4OH-
C. 装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动
D. 放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com