
科目: 来源: 题型:
【题目】某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是
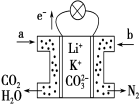
A.a为O2,b为CH4
B.CO 32-向正极移动
C.此电池在常温时也能工作
D.正极电极反应式为2CO2+O2+4e-=2CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,2L密闭容器中装入2 molN2和足量的氢气反应,2 min末时,测得N2为1 mol,该反应的速率表示中,不正确的是( )
A. υ(N2)=0.25 mol·L-1·min-1 B. υ(H2)=0.75 mol·L-1·min-1
C. υ(NH3)=0.5 mol·L-1·min-1 D. υ(N2)=0.5 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】反应mA(固)+nB(气)pC(气)△H<0在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( ) 
A.m+n>P
B.n>p
C.x点表示该反应的正反应速率小于逆反应速率
D.x点比y点时的反应速率慢
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 热稳定性:HI>HBr>HCl B. 元素非金属性:P>S>Cl
C. 原子半径:S>C1>F D. 碱性:Mg(OH)2>KOH
查看答案和解析>>
科目: 来源: 题型:
【题目】分析以下几个热化学方程式,哪个是表示固态碳和气态氢气燃烧时的燃烧热的是( )
A.C(s)+O2(g)═CO(g)△H=﹣110.5 kJ/mol
B.C(s)+O2(g)═CO2(g)△H=﹣393.5 kJ/mol
C.2H2(g)+O2(g)═2H2O(l)△H=﹣571.6 kJ/mol
D.H2(g)+ ![]() ?O2(g)═H2O(g)△H=﹣241.8 kJ/mol
?O2(g)═H2O(g)△H=﹣241.8 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作: A.转移到容量瓶中最终配制成250mL烧碱溶液;
B.用移液管(或碱式滴定管)量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂;
C.在天平上准确称取烧碱样品Wg,在烧杯中加蒸馏水溶解;
D.将物质的量浓度为Mmol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度数为V1mL;
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2mL.
请完成下列问题:
(1)操作步骤的正确顺序是(填写字母)→→→→
(2)滴定至终点时,锥形瓶内溶液的pH约为 , 终点时溶液颜色变化是
(3)若酸式滴定管没有用标准H2SO4溶液润洗,会对测定结果有何影响(填“偏高”、“偏低”或“无影响”,其他操作均正确)
(4)该烧碱样品的纯度计算式是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度(T℃)下的溶液中,c(H+)=10﹣x molL﹣1 , c(OH﹣)=10﹣y molL﹣1 , x与y的关系如图所示,请回答下列问题: 
(1)此温度下,水的离子积Kw为 , 则该温度T25(填“>”、“<”或“=”).
(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示.
实验序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | 7 |
③ | 22.00 | 22.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则a= , 实验②中由水电离产生的c(OH﹣)=molL﹣1.
(3)在此温度下,将0.1molL﹣1的NaHSO4溶液与0.1molL﹣1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
甲 | 乙 | 丙 | 丁 | |
0.1molL﹣1 Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
0.1molL﹣1 NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
①按丁方式混合后,所得溶液显(填“酸”、“碱”或“中”)性.
②写出按乙方式混合后,反应的离子方程式: .
③按甲方式混合后,所得溶液的pH为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】反应3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
A.保持体积不变,增加H2O(g)的物质的量
B.将容器的体积缩小一半
C.保持体积不变,充入Ar使压强增大
D.保持压强不变,充入Ar使体积增大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列在理论上可设计成原电池的化学反应是( )
A. C(s)+H2O(g)=CO(g)+H2 (g)
B. Ba(OH)28H2O(s)+2NH4C1(s)=BaCl2(aq)+2NH3H2O(l)+8H2O(l)
C. C(s)+CO2(g)=2CO(g)
D. CH4(g)+2O2(g)→CO2(g)+2H2O(l)
查看答案和解析>>
科目: 来源: 题型:
【题目】氮的固定是几百年来科学家一直研究的课题.
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值.
反应 | 大气固氮 | 工业固氮 | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.84×10﹣31 | 0.1 | 5×108 | 0.507 | 0.152 |
①分析数据可知:大气固氮反应属于(填“吸热”或“放热”)反应
②分析数据可知:人类不适合大规模模拟大气固氮原因
③从平衡角度考虑.工业固氮应该选择常温条件,但实际工业产生却选择500℃左右的高温,解释其原因
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是(填“A”或“B”);比较р1、р2的大小关系 . 
(3)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1)4NH3(g)+3O2(g),则其反应热△H= . 已知:N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJmol﹣1
2H2(g)+O2(g)2H2O(l)△H=﹣571.6kJmol﹣1 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com