
科目: 来源: 题型:
【题目】下列各组物质中,被氧化与被还原的物质的物质的量之比为1:2的是( )
A.Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
B.SO2+2H2S═3S+2H2O
C.3NO2+H2O═2HNO3+NO
D.3S+6KOH═2K2S+K2SO3+3H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为长式周期表的一部分,其中的编号代表对应的元素。
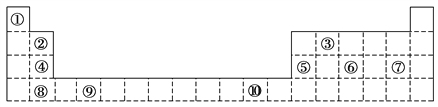
请回答下列问题:
(1)表中属于d区元素的是________(填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为________;③和⑦形成的一种常见溶剂的化学式为________,其密度比水________。
(3)元素⑥原子的外围电子排布图为________;该元素与同主族相邻元素的氢化物的稳定性从大到小为________________ 。
(4)元素①的第一电离能________元素③(选填“>”、“=”或“<”)的第一电离能;元素⑥的电负性________元素⑦(选填“>”、“=”或“<”)的电负性。
(5)元素⑦和⑧形成的化合物的电子式为________。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质用途的说法,错误的是( )
A.过氧化钠可用作潜水艇里氧气的来源B.甲醛可用作食物的防腐剂
C.柠檬黄可作食品添加剂中的着色剂D.小苏打可用作食品的疏松剂
查看答案和解析>>
科目: 来源: 题型:
【题目】化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中,不正确的是( )
A. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
B. 明矾水解的离子方程式: Al3++ 3 H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
C. 以石墨作电极电解氯化铝溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D. 硫化氢在水溶液中的电离方程式:H2S + H2O![]() HS- + H3O+
HS- + H3O+
查看答案和解析>>
科目: 来源: 题型:
【题目】改变0.1![]() 二元弱酸
二元弱酸![]() 溶液的pH,溶液中的
溶液的pH,溶液中的![]() 、
、![]() 、
、![]() 的物质的量分数
的物质的量分数![]() 随pH的变化如图所示[已知
随pH的变化如图所示[已知 ]。
]。

下列叙述错误的是( )
A. pH=1.2时, ![]()
B. ![]()
C. pH=2.7时, ![]()
D. pH=4.2时, ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】可降解塑料PCL的结构可表示为 ![]() .其合成路线如下.
.其合成路线如下. 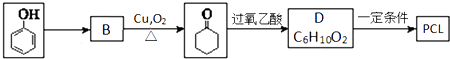
已知:
① ![]()
②R﹣CH=CH﹣CH3 ![]() R﹣CH=CH﹣CH2Br
R﹣CH=CH﹣CH2Br
③ ![]()
回答下列问题:
(1)由苯酚生成B的反应试剂和条件为
(2)D的结构简式是 . 上述生成D的反应类型是 .
(3)PCL属于(填“线型”或“体型”)高分子材料. 与D具有相同官能团的同分异构体E经下列合成路线可转化为D.![]()
(4)E的结构简式是 .
(5)由H生成K的化学方程式是 .
(6)M的氧化产物己二酸是合成尼龙的原料之一,用B做原料三步反应可制得己二酸. B﹣W→X→己二酸
写出W、X的结构简式:W、X
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是某学生为探究AgCl沉淀转化为Ag2S沉淀的反应所做实验的记录.
步 骤 | 现 象 |
Ⅰ.取5mL 0.1mol/L AgNO3与一定体积0.1mol/L NaCl溶液,混合,振荡. | 立即产生白色沉淀 |
Ⅱ.向所得悬浊液中加入2.5mL 0.1mol/L Na2S溶液. | 沉淀迅速变为黑色 |
Ⅲ.将上述黑色浊液,放置在空气中,不断搅拌. | 较长时间后,沉淀变为乳白色 |
Ⅳ.滤出Ⅲ中的乳白色沉淀,加入足量HNO3溶液. | 产生红棕色气体,沉淀部分溶解 |
Ⅴ.过滤得到滤液X和白色沉淀Y;向X中滴加Ba(NO3)2溶液. | 产生白色沉淀 |
(1)为了证明沉淀变黑是AgCl转化为Ag2S的缘故,步骤I中NaCl溶液的体积范围为 .
(2)已知:25℃时Ksp(AgCl)=1.8×10﹣10 , Ksp(Ag2S)=6×10﹣30 , 此沉淀转化反应的平衡常数K .
(3)步骤V中产生的白色沉淀的化学式为 , 步骤Ⅲ中乳白色沉淀除含有AgCl外,还含有 .
(4)为了进一步确认步骤Ⅲ中乳白色沉淀产生的原因,设计了如下图所示的对比实验装置. ①装置A中玻璃仪器有圆底烧瓶、导管和 , 试剂W为 .
②装置C中的试剂为NaCl溶液和Ag2S悬浊液的混合物,B中试剂为 .
③实验表明:C中沉淀逐渐变为乳白色,B中没有明显变化.
完成C中反应的化学方程式:
Ag2S+NaCl++AgCl+S+
C中NaCl的作用是: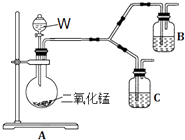
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A.1mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1mol任何物质体积均为22.4L
查看答案和解析>>
科目: 来源: 题型:
【题目】天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)、乙硫醇(C2H5SH)],可以用氢氧化钠溶液洗涤除去.
(1)硫元素的原子结构示意图为;羰基硫分子的电子式为 .
(2)下列说法正确的是 . a.乙硫醇的相对分子质量大于乙醇,故其沸点更高
b.同温度同浓度下Na2CO3溶液的pH大于Na2SO4溶液,说明硫元素非金属性强于碳元素
c.H2S分子和CO2都是极性分子,因为它们都是直线形分子
d.由于乙基的影响,乙硫醇的酸性弱于H2S
(3)羰基硫用氢氧化钠溶液处理及利用的过程如下(部分产物已略去): COS ![]() Na2S溶液
Na2S溶液 ![]() X溶液+H2
X溶液+H2
①反应I除生成两种正盐外,还有水生成,其化学方程式为 .
②已知X溶液中硫元素的主要存在形式为S2O32﹣ , 则Ⅱ中主要反应的离子方程式为 .
③如图是反应Ⅱ中,在不同反应温度下,反应时间与H2产量的关系图(Na2S初始含量为3mmo1).
a.判断T1、T2、T3的大小:;
b.在T1温度下,充分反应后,若X溶液中除S2O32﹣外,还有因发生副反应而同时产生的SO42﹣ , 则溶液中c(S2O32﹣):c(SO42﹣)= . 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com