
科目: 来源: 题型:
【题目】常温下,向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(稀溶液混合时体积可直接相加)。下列判断错误的是
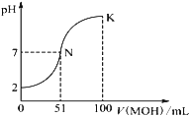
A. 由图中信息可知,HA一定是强酸
B. 当V(MOH)=50.00 mL时,混合溶液中c(M+)+c(MOH)=0.01 mol·L-1
C. N点对应的溶液中c(M+)=c(A-)
D. K点所对应的溶液中离子浓度大小关系为:c(M+)>c(A-)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.化学反应的焓变与反应的途径有关
B.室温下,稀释0.1molL﹣1CH3COOH溶液,溶液的导电能力减弱
C.常温常压下,22.4L Cl2中含有的分子数为6.02×1023个
D.等质量的铜按a、b两种途径完全转化为Cu(NO3)2 , 途径a、b消耗的硝酸一样多![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解.实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2 , 实验装置如图所示. 
当溶液pH约为4时,停止反应.在20℃左右静置结晶.生成Na2S2O5的化学方程式为:2NaHSO3═Na2S2O5+H2O
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2 , 其离子方程式为 .
(2)装置Y的作用是
(3)析出固体的反应液经减压抽滤、洗涤、25℃﹣30℃干燥,可获得Na2S2O5固体.
①组成减压抽滤装置的主要仪器是布氏漏斗、和抽气泵.
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体.用饱和SO2水溶液洗涤的目的是 .
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4 , 其可能的原因是
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下发生下列反应,其中属于盐类水解反应的是
A. Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
B. HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
C. HS-+H+![]() H2S
H2S
D. NH4++2H2O![]() NH3·H2O+H3O+
NH3·H2O+H3O+
查看答案和解析>>
科目: 来源: 题型:
【题目】由徐光宪院士发起、院士学子同创的《分子共和国》科普读物最近出版了,全书形象生动地戏说了BF3、TiO2、HCHO、N2O、二茂铁、NH3、HCN、H2S、O3、异戊二烯和萜等众多“分子共和国”中的明星.
(1)写出Fe3+的基态核外电子排布式 .
(2)HCHO分子中碳原子轨道的杂化轨道类型为;1mol HCN分子中含有σ键的数目为mol.
(3)N2O的空间构型为 , 与N2O互分等电子体的一种离子为 .
(4)TiO2的天然晶体中,最稳定的一种晶体结构如图,则黑球表示原子. 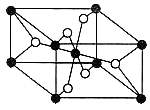
查看答案和解析>>
科目: 来源: 题型:
【题目】数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果.如利用CO2和CH4重整可制合成气(主要成分为CO、H2),已知重整过程中部分反应的热化学方程式为:
I、CH4(g)═C(s)+2H2(g)△H=+75.0kJmol﹣1
II、CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41.0kJmol﹣1
III、CO(g)+H2(g)═C(s)+H2O(g)△H=﹣131.0kJmol﹣1
(1)反应CO2(g)+CH4(g)═2CO(g)+2H2(g)的△H=kJmol﹣1 .
(2)固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲. 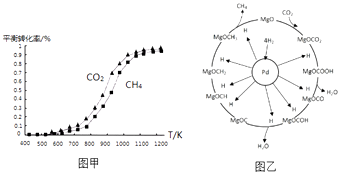
①同温度下CO2的平衡转化率(填“大于”或“小于”)CH4的平衡转化率,其原因是
②高温下进行该反应时常会因反应I生成“积碳”(碳单质),造成催化剂中毒,高温下反应I能自发进行的原因是 .
(3)一定条件下Pd﹣Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图乙所示,该反应的化学方程式为
(4)CO常用于工业冶炼金属,如图是在不同温度下CO还原四种金属氧化物达平衡后气体中lg[c(CO)/c(CO2)]与温度(t)的关系曲线图.下列说法正确的是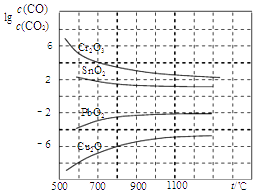
A.工业上可以通过增高反应装置来延长矿石和
CO接触的时间,减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属铬(Cr)
C.工业冶炼金属铜(Cu)时较低的温度有利于
提高CO的利用率
D.CO还原PbO2的反应△H>0
(5)在载人航天器中应用电化学原理,以Pt为阳极,Pb(CO2的载体)为阴极,KHCO3溶液为电解质溶液,还原消除航天器内CO2同时产生O2和新的能源CO,总反应的化学方程式为:2CO2 ![]() 2CO+O2 , 则其阳极的电极反应式为 .
2CO+O2 , 则其阳极的电极反应式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】关于过滤操作的描述,不正确的是
A. 滤纸应紧贴漏斗内壁并用少量水润湿,使滤纸与漏斗壁之间没有气泡
B. 漏斗内的过滤液的液面应高于滤纸边缘
C. 要沿着玻璃棒慢慢向漏斗中倾倒过滤液
D. 漏斗下端管口应紧靠烧杯内壁
查看答案和解析>>
科目: 来源: 题型:
【题目】在0.1mol/L的NH3·H2O溶液中存在如下电离平衡:NH3·H2O![]() NH4++OH-对于该平衡,下列叙述正确的是
NH4++OH-对于该平衡,下列叙述正确的是
A. 加入少量NaOH固体,溶液中c(OH-)减少
B. 通入少量HCl气体,平衡向正反应方向移动
C. 加入少量水,平衡向逆反应方向移动
D. 加入少量NH4Cl固体,平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组用下图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去). 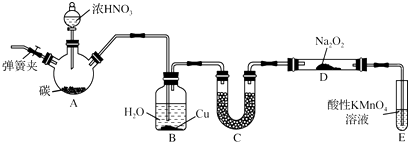
(1)【背景素材】
①2NO+Na2O2═2NaNO2;
②NO能被酸性KMnO4氧化成NO3﹣ , MnO4﹣被还原为Mn2+ .
③在酸性条件下NaNO2能把I﹣氧化为I2;S2O32﹣能把I2还原为I﹣ .
【制备NaNO2】
(i)装置A三颈烧瓶中发生反应的化学方程式为 .
(ii)B装置的目的是① , ② .
(iii)为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是(填序号).
A.P2O5 B.碱石灰 C.无水CaCl2 D.生石灰
(iv)E装置的作用是 .
(2)【测定NaNO2纯度】
可供选择的试剂有:
A.稀硫酸 B.c1 molL﹣1 KI溶液 C.淀粉溶液 D.c2 molL﹣1 Na2S2O3溶液
E.c3 molL﹣1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,可选择的试剂是(填序号).
②利用NaNO2的氧化(请补充完整实验步骤).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com