
科目: 来源: 题型:
【题目】某研究性学习小组探究碳化铝的性质:发现碳化铝与水在常温下剧烈反应,生成大量气体和白色沉淀,该沉淀既能溶于盐酸也能溶于NaOH溶液,该小组同学为了探究气体产物的组成,设计出如图1所示实验:
(1)利用碳化铝制取气体,图2装置中适合作为气体发生装置的是 . 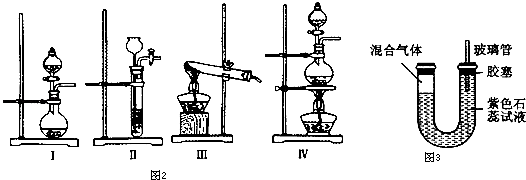
(2)正确选择发生装置后,连接装置进行实验.一段时间后,硬质玻璃管C中黑色粉末变成红色,干燥管D中白色粉末变成蓝色,装置E中澄清石灰水变浑浊,尾气燃烧产生蓝色火焰.①干燥管D中的试剂可能是 , 其作用是 .
②根据实验现象,某同学得出下列推论,其中正确的是 .
a.气体与氧化铜在一定条件下反应,氧化产物只有二氧化碳
b.气体与氧化铜在一定条件下反应,产物一定有水和二氧化碳,可能有一氧化碳
c.气体与氧化铜在一定条件下反应,产物一定有水、二氧化碳和一氧化碳
d.气体具有还原性,氧化产物可能有多种
(3)实验完毕后,要先后熄灭C和F处的酒精灯,应后熄灭的是处酒精灯,理由是 .
(4)若最后在F处点燃气体与在A处产生的气体相同,实验前系统内的空气已排尽,实验验结束后,C装置减轻12.8g,D装置增重7.2g,E装置增重8.8g(假定D、E吸收气体是完全的),则A、C处发生反应的方程式分别为、 .
(5)如图3所示,U型透明玻璃管的左端封闭有A处产生气体和氯气的混合气,将该装置放在日光灯下.一段时间后(不考虑水与氯气的反应),下列关于U型管中可能出现的现象的叙述中正确的是a.U型管左侧会有油状液滴出现
b.溶液很快变成蓝色
c.气柱缩小,右端液柱下降
d.气柱膨胀,右端玻璃管中液体溢出.
查看答案和解析>>
科目: 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴体的装置示意图及有关数据如表:
苯 | 溴 | 溴苯 | |
密度/gcm﹣3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑.在b中小心加入4.0mL液态溴.再将b中的液溴慢慢加入a中,充分反应.装置a中主要反应:;装置d的作用 .
(2)反应过程中,a外壁温度升高.为提高原料的利用率,可采取以下措施:
①采用装置c进行冷凝回流,回流的主要物质有 .
②利用温度计控制温度,适宜的温度范围为(填序号).
A.>156℃B.59℃﹣80℃C.<59℃
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL 10%的NaOH溶液、10mL水洗涤.
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.
步骤②中NaOH溶液洗涤的主要作用是(用化学方程式表示);
(4)经以上分离操作后,粗溴苯中还含有的主要杂质为 , 要进一步提纯,下列操作中必须的是(填序号).
A.分液 B.过滤 C.蒸馏 D.萃取
(5)在该实验中,a的容积最适合的是(填序号).
A.25mL
B.50mL
C.250mL
D.500mL
查看答案和解析>>
科目: 来源: 题型:
【题目】在淀粉KI溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失.下列对该实验原理的解释和所得结论错误的是( )
A.第一步反应的离子方程式为ClO﹣+2I﹣+2H+═I2+Cl﹣+H2O
B.淀粉KI溶液变蓝是因为I﹣被氧化为I2 , 淀粉遇I2变蓝色
C.蓝色逐渐消失的原因是Na2SO3溶液具有漂白性
D.微粒的氧化性由强到弱的顺序是ClO﹣>I2>SO ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】氮、硫、碳的氧化物有多种,其中SO2和NOx都是大气污染物,对它们的研究有助于空气的净化.
(1)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g) K1△H1<0 (Ⅰ)
2NO(g)+Cl2(g)2ClNO(g) K2△H2<0 (Ⅱ)
4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=(用K1、K2表示).
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2 , 10min时反应(II)达到平衡.测得10min内v(ClNO)=7.5×10﹣3molL﹣1min﹣1 , NO的转化率α1= . 其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2α1(填“>”“<”或“=”).
(3)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究小组在实验室以Ag﹣ZSM﹣5为催化剂,测得NO转化为N2的转化率随温度变化的情况如图1.
①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为;在 ![]() =1的条件下,应控制的最佳温度在左右.
=1的条件下,应控制的最佳温度在左右.
②NO2尾气常用NaOH溶液吸收,生成NaNO3和 NaNO2 . 已知NO2﹣的水解常数K=2×10﹣11molL﹣1 , 常温下某NaNO2和 HNO2 混合溶液的PH为5,则混合溶液中c(NO2﹣)和c(HNO2)的比值为
(4)利用图2所示装置(电极均为惰性电极)也可吸收SO2 , 并用阴极排出的溶液吸收NO2 . 阳极的电极反应式为在碱性条件下,用阴极排出的溶液吸收NO2 , 使其转化为无害气体,同时有SO42﹣生成.该反应的离子方程式为
(5)消除汽车尾气,可以通过反应2NO(g)+2CO(g)2CO2(g)+N2(g).当质量一定时,增大固体催化剂的表面积可提高化学反应速率.如图3表示在其他条件不变时,NO的浓度c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线.①该反应的△H(填“>”或“<”)0.
②若催化剂的表面积S1>S2 , 在右图中画出c(NO)在T1、S2条件下达到平衡过程中的变化曲线(并作相应标注).
(6)某研究性学习小组欲探究SO2能否与BaCl2溶液反应生成BaSO3沉淀.查阅资料得知常温下BaSO3的KSP为5.48×10﹣7 , 饱和亚硫酸中c(SO32﹣)=6.3×10﹣8 molL﹣1 . 将0.1molL﹣1的BaCl2溶液滴入饱和亚硫酸中,(填“能”或“不能”)生成BaSO3沉淀,原因是(请写出必要的推断过程).
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2 .
(1)A分子的质谱图如图所示,从图中可知其相对分子质量是90,则A的分子式是
(2)A能与NaHCO3溶液发生反应,A一定含有的官能团名称是
(3)A分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则A的结构简式是 .
(4)0.1mol A与足量Na反应,在标准状况下产生H2的体积是L.
(5)A在一定条件下可聚合得到一种聚酯,用于制造手术缝合线,其反应的化学方程式是 . 
查看答案和解析>>
科目: 来源: 题型:
【题目】某元素原子的核电荷数是电子层数的五倍,其质子数是最外层电子数的三倍,该元素的原子核外电子排布是( )
A. 2、5B. 2、7C. 2、8、5D. 2、8、7
查看答案和解析>>
科目: 来源: 题型:
【题目】氟、氯、溴、碘四种元素,下列有关它们的性质递变规律的说法,不正确的是( )
A. 单质的密度依次增大
B. 单质的熔点和沸点依次升高
C. 氯气可从碘化钾溶液中置换出碘
D. 溴单质可从氯化钠溶液中置换出氯
查看答案和解析>>
科目: 来源: 题型:
【题目】有一种有机物X的键线式如图所示.
(1)X的分子式为 .
(2)有机物Y是X的同分异构体,且属于芳香族化合物,则Y的结构简式是 .
(3)Y在一定条件下可生成高分子化合物,该反应的化学方程式是 .
(4)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有种. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com