
科目: 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目: 来源: 题型:
【题目】原子序数依次递增的甲、乙、丙、丁、戊是周期表中前30号元素,其中甲、乙、丙三元素的基态原子2p能级都有单电子,单电子个数分别是2、3、2;丁与戊原子序数相差18,戊元素是周期表中ds区的第一种元素。回答下列问题:
(1)甲能形成多种常见单质,在熔点很高的两种常见单质中,原子的杂化方式分别为______、__________。
(2)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有I3、I4、I5…,推测丁元素的电离能突增应出现在第________电离能。
(3)戊的基态原子有________种形状不同的原子轨道;
(4)甲、乙分别都能与丙形成原子个数比为 1:3的微粒,则该两种微粒的空间构型分别为:_________________ ;__________________。
(5)丙和丁形成的一种离子化合物的晶胞结构如右图,该晶体中阳离子的配位数为_________ 。距一个阴离子周围最近的所有阳离子为顶点构成的几何体为_______________。已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,该化合物的相对分子质量为 M,则该晶胞中黑球的半径r =_____cm。(用含ρ、NA的计算式表示)
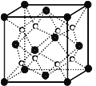
查看答案和解析>>
科目: 来源: 题型:
【题目】电解原理在化学工业中有广泛应用.图1表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: 
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则: ①X是极(填“阴”或“阳”),X极逸出(填“黄绿色”或“无色”)气体,同时X极附近溶液呈色.
②电解池中Y极上的电极反应式为 . X极上的电极反应式为 .
(2)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼(得到纯铜),电解液a选用CuSO4溶液,则: ①Y电极的材料是(填“粗铜”或“纯铜”).
②X电极的电极反应式是 .
③下列说法正确的是 .
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(3)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4 , 若将该反应设计为电解池,其电解质溶液需用 , 阳极材料是用 , 阴极电极反应式为
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,还原剂与氧化剂的质量比和物质的量之比不相同的是( )
A.常温下用NaOH溶液吸收Cl2
B.Na在空气中燃烧
C.Na2O2吸收CO2
D.S在空气中燃烧
查看答案和解析>>
科目: 来源: 题型:
【题目】硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgOB2O3H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如图: 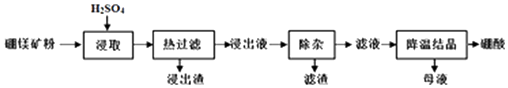
已知:i.Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4.
ⅱ.H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g.
(1)为了提高硼镁矿粉的浸出率,可采取的措施有(至少答两条).
(2)“浸出液”显酸性,含H3BO3和Mg2+、SO42﹣ , 还含有Fe3+、Fe2+、Ca2+、Al3+等杂质.“除杂”时向浸出液中依次加入适量H2O2和MgO,H2O2的作用是(用离子方程式表示),MgO除去的杂质离子是 .
(3)已知H3BO3与过量的NaOH反应生成Na[B(OH)4],试写出H3BO3在溶液中的电离方程式 .
(4)“浸取”后,采用“热过滤”的目的是 , 母液中的主要溶质有 .
(5)测定所得产品的纯度:取a g硼酸,小心加热使其分解脱去水分(杂质受热不分解),得残留固体b g,则产品的纯度为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】组成蛋白质的元素主要有C、H、O、N及S、P和少量的Zn、Cu等.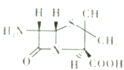
(1)N、P、S的第一电离能由小到大的顺序为 .
(2)组成蛋白质的最简单的氨基酸(HOOCCH2NH2)介子中,π键数目为 .
(3)Zn2+、Cu2+能与NH3、H2O、Cl﹣等形成配位数为4的配合物.①基态Zn2+的价电子(外围电子)排布式为 .
②[Zn(H2O)4]SO4中不存在的化学键类型有 . (填序号).
a.配位键 b.金属键 c.共价键 d.氢键 e.离子键
③[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl﹣取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 .
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(4)由上述几种元素组成的6一氨基青霉烷酸的结构如图,其中采用sp3杂化的原子除了S外,还有 .
(5)紫外光的光子所具有的能量约为399kJmol﹣根据下表有关蛋白质分子中主要化学键的键能信息,说明人体长时间照射紫外光后皮肤易受伤害的原因是(填序号).
共价键 | C﹣C | C﹣N | C﹣S |
键能/(kJmol﹣1) | 347 | 305 | 259 |
查看答案和解析>>
科目: 来源: 题型:
【题目】据报道,近来发现了一种新的星际分子氰基辛炔,其结构简式为HC≡C—C≡C—C≡C—C≡C—C≡N。下列对该物质的判断正确的是( )
A.属于不饱和烃
B.不能使酸性KMnO4溶液褪色
C.所有原子都在同一条直线上
D.可由乙炔和含氮化合物加聚制得
查看答案和解析>>
科目: 来源: 题型:
【题目】含苯酚的工业废水处理的流程图如图所示: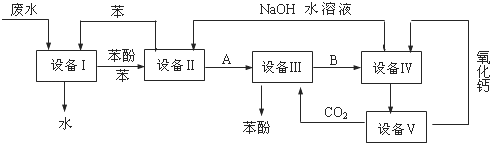
(1)上述流程里,设备Ⅰ中进行的是操作(填操作名称),实验室里这一步操作可以用进行(填仪器名称).
(2)由设备Ⅱ进入设备Ⅲ的物质A是 , 由设备Ⅲ进入设备Ⅳ的物质B是
(3)在设备Ⅲ中发生反应的化学方程式为
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和 , 通过操作(填操作名称)可使产物相互分离.
(5)图中,能循环使用的物质是C6H6、CaO、 .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知Mg2C3的结构与CaC2相似,由此可断定Mg2C3与水反应的产物是( )
A.Mg(OH)2和CH≡CH
B.MgO和CH≡CH
C.Mg(OH)2和CH3CH=CH2
D.Mg(OH)2和CH3C≡CH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com