
科目: 来源: 题型:
【题目】在中和热的实验测定中,下列操作中使结果偏高的是
A.实验装置保温、隔热效果差
B.量取酸碱溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目: 来源: 题型:
【题目】从柑桔中可提炼出苧烯 ![]() .下列关于苧烯的说法中,正确的是( )
.下列关于苧烯的说法中,正确的是( )
A.分子式为C10H16 , 是1,3﹣丁二烯的同系物
B.其分子内所有的碳原子均在同一平面上
C.与过量的Br2的CCl4 溶液反应的产物为: 
D.易溶于水,且能发生加聚反应生成高分子化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】铝自然形成的氧化膜易脱落.以硫酸为电解液,分别以石墨和铝材做阴、阳极材料,经过电解处理形成的氧化铝膜,抗蚀能力强.其制备的简要流程如图.下列用来解释流程中反应的方程式不正确的是( ) 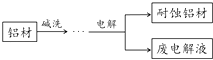
A.碱洗目的是除去铝材表面的自然氧化膜:2OH﹣+Al2O3═2AlO2﹣+H2O
B.碱洗时铝材表面会出现气泡:2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑
C.获得耐蚀铝材的电极反应为:4Al﹣12e﹣+3O2═2Al2O3
D.用稀氨水洗去耐蚀铝材表面的酸:NH3H2O+H+═NH4++H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A.沸点:正戊烷>2﹣甲基丁烷>丙烷
B.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
C.相对分子质量相近的醇比烷烃沸点高是因为醇分子间存在氢键
D.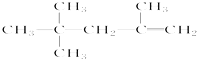 的名称为2,2,4﹣三甲基﹣4﹣戊烯
的名称为2,2,4﹣三甲基﹣4﹣戊烯
查看答案和解析>>
科目: 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应:Cu+2H2SO4(浓)═CuSO4+SO2↑+2H2O
试通过计算和推理完成下面的问题:
(1)SO2物质可以使酸性KMnO4溶液褪色,此反应中(填写化学式)失去电子.
(2)足量的铜片与 含溶质1.8mol的浓H2SO4充分反应,如果该反应过程中转移了 0.2mol电子,生成的CuSO4的质量为克,生成的气体在标准状况下体积为升(假设气体全部逸出).
(3)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应.请写出此过程发生的反应的离子方程式: .
查看答案和解析>>
科目: 来源: 题型:
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体.相应的实验过程如图:
(1)写出上述实验过程中所用试剂(写化学式):
试剂①;试剂③ .
(2)判断试剂①已过量的方法是: .
(3)用化学方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯.操作①的实验结果:淀粉(填“能”或“不能”)透过半透膜;SO42﹣(填“能”或“不能”)透过半透膜;请用实验证明上述结果,完成下表(可不填满,也可增加):限选试剂:1mol/L AgNO3溶液、1mol/L BaCl2溶液、1mol/L Ba(NO3)2溶液、碘水、稀盐酸、稀硝酸
编号 | 实验操作 | 预期现象和结论 |
① | ||
② | ||
查看答案和解析>>
科目: 来源: 题型:
【题目】2011年9月16日是“国际保护臭氧层日”,其主题是“淘汰氟氯烃:绝佳机会”。为了保护臭氧层,可采取的有效措施是( )
A.减少二氧化硫的排放量
B.减少含铅废气的排放量
C.减少氟氯代烷的排放量
D.减少二氧化碳的排放量
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是(填序号),本实验所需玻璃仪器E规格为mL.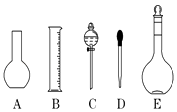
(2)下列操作中,容量瓶所不具备的功能有(填序号).
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶
D.量取一定体积的液体
(3)在配制NaOH溶液实验中,其他操作均正确.若定容时仰视刻度线,则所配制溶液浓度0.1mol/L (填“大于”“等于”或“小于”,下同).若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度0.1mol/L.
(4)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为 mL(计算结果保留一位小数).如果实验室有10mL、25mL、50mL量筒,应选用 mL规格的量筒最好.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com